题目内容
15.已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是( )| A. | 该反应中FeSO4只做还原剂,Na2O2只做氧化剂 | |
| B. | 4 mol Na2O2在反应中共得到8NA个电子 | |
| C. | 该反应中由4 mol Fe2+还原的Na2O2是3 mol | |
| D. | 反应中氧化剂与还原剂的物质的量之比为3:5 |
分析 由4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,可知Fe元素的化合价由+2价升高为+3价,过氧化钠中O元素的化合价由-1价升高为0,由-1价降低为-2价,该反应中转移电子数为6e-,以此来解答.
解答 解:A.过氧化钠中O元素的化合价由-1价升高为0,由-1价降低为-2价,所以过氧化钠既是氧化剂也是还原剂,故A错误;
B.有4molNa2O2完全反应时转移6 mol电子,故B错误;
C.由反应及元素的化合价变化可知,生成4molFe(OH)3时转移6 mol电子,故C错误;
D.Fe、O元素的化合价升高,O元素的化合价降低,则还原剂是FeSO4、Na2O2,氧化剂是Na2O2,反应中氧化剂与还原剂的物质的量之比为(4-1):(4+1)=3:5,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子数的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
相关题目
2.下列各项中离子方程式的书写与反应物的用量无关的是( )
| A. | Ba(OH)2溶液与H2SO4溶液 | B. | Ba(HCO3)2溶液与NaOH溶液 | ||
| C. | 盐酸与K2CO3溶液 | D. | FeBr2溶液与Cl2 |
3.关于下列词句或谚语,说法不正确的是( )
| A. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| B. | “曾青得铁化为铜”发生了置换反应 | |
| C. | “春蚕到死丝方尽”中的“丝”的和“慈母手中线,游子身上衣”中的棉“线”主要成分都是纤维素 | |
| D. | “卤水点豆腐,一物降一物”的前半句话与胶体知识有关 |
3.下列化学式与指定物质的俗名对应正确的是( )
| A. | CH3COOH--酒精 | B. | CO--水煤气 | C. | CaSO3--大理石 | D. | Na2CO3--纯碱 |
10.碱性电池具有容量大,放电电流大的特点,因而得到广泛的应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn+2MnO2+2H2O═Zn(OH)2+MnOOH,下列说法不正确的是( )
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
7.属于芳香族,且苯环上一氯代物有4种的是( )
| A. | CH2=CH-CH=CH2 | B. | CH3CH=CH2 | C. | 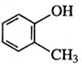 | D. | 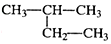 2-甲基丁烷 2-甲基丁烷 |
5.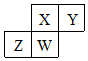 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
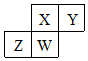 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Y、Z、W的最高化合价分别与其主族序数相等 | |
| C. | 最简单气态氢化物的热稳定性:X>Z>W | |
| D. | 最高价氧化物对应水化物的酸性:X>Z>W |
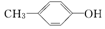 ;③C2H5OH;④CH3CH2Br;⑤CCl4;⑥CH3COOCH3;⑦CH3COOC2H5.据官能团的不同可分为( )
;③C2H5OH;④CH3CH2Br;⑤CCl4;⑥CH3COOCH3;⑦CH3COOC2H5.据官能团的不同可分为( )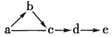 其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.
其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.