题目内容
25℃时将水不断滴入0.1mol/L的氨水中,下列变化的图象合理的是( )
分析:25℃时将水不断滴入0.1mol/L的氨水中,一开始起决定因素的是浓度,溶液越稀,PH下降得越快,不呈一次函数是因为氨水是弱碱,越稀越电离,但是浓度起主要作用.在拐点处,浓度不断下降,电离起主要作用.后面PH的变化肯定是越来越慢 因为不管怎么稀释 PH只能越来越接近7却达不到7,所以pH会越降越慢;
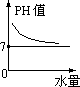
A、稀释时氢氧根离子浓度下降,pH下降,趋近于7;
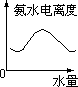
B、加入水电离度始终增大;
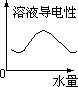
C、离子浓度下降,导电能力下降;
D、温度一定溶液中存在离子积常数,氢氧根离子浓度下降,氢离子浓度增大,最后基本不变.
A、稀释时氢氧根离子浓度下降,pH下降,趋近于7;
B、加入水电离度始终增大;
C、离子浓度下降,导电能力下降;
D、温度一定溶液中存在离子积常数,氢氧根离子浓度下降,氢离子浓度增大,最后基本不变.
解答:解:A、稀释时氢氧根离子浓度下降,pH下降,趋近于7,不能低于7,故A正确;
B、弱电解质加水稀释过程中,促进电离,电离度始终增大,故B错误;
C、溶液导电能力取决于离子浓度大小,加水稀释离子浓度下降,导电能力下降,故C错误;
D、温度一定,溶液中 存在离子积常数,氢氧根离子浓度下降,氢离子浓度增大,最后基本不变,故D错误;
故选A.
B、弱电解质加水稀释过程中,促进电离,电离度始终增大,故B错误;
C、溶液导电能力取决于离子浓度大小,加水稀释离子浓度下降,导电能力下降,故C错误;
D、温度一定,溶液中 存在离子积常数,氢氧根离子浓度下降,氢离子浓度增大,最后基本不变,故D错误;
故选A.
点评:本题考查了弱电解质稀释过程中的分析判断,主要是溶液导电性的分析依据,溶液中离子浓度变化的判断,题目难度中等.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目





 的氨水中,下列变化的图象合理的是
的氨水中,下列变化的图象合理的是