题目内容
18.某有机样品3.0g完全燃烧,将燃烧后的混合物通入过量的澄清石灰水中,石灰水共增重6.2g,经过滤得到10g沉淀.该有机样品的组成可能是(括号内给出的是有机物的分子式)( )| A. | 葡萄糖(C6H12O6)与蔗糖(C12H22O11) | B. | 醋酸与甲酸甲酯(C2H4O2) | ||
| C. | 乙醇与甲醛(CH2O) | D. | 二甲醚(C2H6O)与乳酸(C3H6O3) |
分析 石灰水增重为燃烧生成CO2和H2O的总质量,10g沉淀为碳酸钙质量,计算碳酸钙物质的量,根据碳原子守恒可得二氧化碳物质的量,进而计算水的物质的量,再结合有机物总质量计算含有氧原子质量,进而计算有机物实验式,结合选项判断.
解答 解:3.0 g有机样品燃烧生成CO2和H2O的总质量为6.2 g,10 g碳酸钙的物质的量为$\frac{10g}{100g/mol}$=0.1 mol,则CO2的物质的量为0.1 mol,
故生成水的质量为6.2 g-0.1 mol×44 g•mol-1=1.8 g,其物质的量为$\frac{1.8g}{18g/mol}$=0.1 mol,含0.2 mol H,
因此,3.0 g样品中氧原子的质量为3.0 g-0.1 mol×12 g•mol-1-0.2 mol×1 g•mol-1=1.6 g,其物质的量为$\frac{1.6g}{16g/mol}$=0.1 mol,
故有机物分子中N(C):N(H):N(O)=0.1:0.2:0.1=1:2:1,则有机酸实验式为CH2O.
A.葡萄糖与蔗糖的分子式分别为C6H12O6、C12H22O11,蔗糖的实验式不是CH2O,故A错误;
B.醋酸与甲酸甲酯的分子式均为C2H4O2,实验式均为CH2O,故B正确;
C.乙醇与甲醛的分子式分别为C2H6O2、CH2O,乙醇实验式不是CH2O,故C错误;
D.二甲醚(C2H6O)与乳酸(C3H6O3)中二甲醚的实验式不是CH2O,故D错误.
故选B.
点评 本题考查有机物分子式的确定,侧重于学生的分析能力和计算能力的考查,注意把握有机物实验式的确定,难度中等.

练习册系列答案
相关题目
1.有机物 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 2,3,3-三甲基戊烷 | B. | 3,3,4-三甲基已烷 | ||
| C. | 3,3-二甲基-4-乙基戊烷 | D. | 2-乙基-3,3-二甲基-4-乙基戊烷 |
9.下列性质比较结果错误的是( )
| A. | 碳碳键键长:乙烯>苯 | B. | 沸点:正戊烷>异戊烷 | ||
| C. | 相对密度: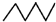 > >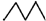 | D. | 水溶性:CH3CH2OH>CH3CH2Br |
13.下列说法正确的是( )
| A. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| B. | 2s的电子云半径比1s电子云半径大,说明2s能级的电子比1s的多 | |
| C. | 1s轨道的电子云形状为圆形的面 | |
| D. | nf能级中最多可容纳14个电子 |
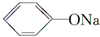 +CH3I→
+CH3I→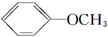 +NaI
+NaI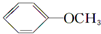 +HI→
+HI→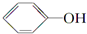 +CH3l
+CH3l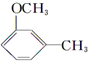 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$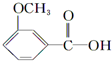
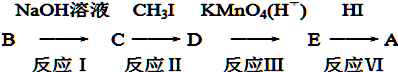
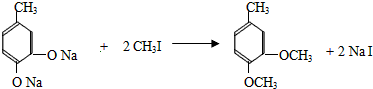 .
. .
.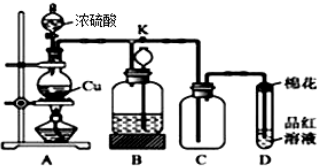
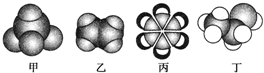
 ,丁CH3CH2OH
,丁CH3CH2OH +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ +H2O
+H2O :回答下列问题:大麻酚的分子式为:C21H26O2,它与足量的溴水反应最多消耗Br23mol.
:回答下列问题:大麻酚的分子式为:C21H26O2,它与足量的溴水反应最多消耗Br23mol.