题目内容
6.下列离子方程式书写正确的是( )| A. | 钠与水:2Na+2H2O═2Na++2 OH-+H2↑ | |
| B. | CaCO3与稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | FeCl3溶液与Fe反应:Fe3++Fe═2Fe2+ |
分析 A.反应生成NaOH和氢气,遵循电子、电荷守恒;
B.碳酸钙在离子反应中保留化学式;
C.一水合氨在离子反应中保留化学式;
D.电子、电荷不守恒.
解答 解:A.钠与水的离子反应为2Na+2H2O═2Na++2 OH-+H2↑,故A正确;
B.CaCO3与稀盐酸的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故B错误;
C.AlCl3溶液中加入足量的氨水的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故C错误;
D.FeCl3溶液与Fe反应的离子反应为2Fe3++Fe═3Fe2+,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
16.下列溶液中,SO42-的物质的量浓度最大的是( )
| A. | 7.5 mL 2 mol•L-1KAl(SO4)2溶液 | B. | 30 mL 1 mol•L-1 MgSO4溶液 | ||
| C. | 20 mL 0.5 mol•L-1Al2(SO4)3溶液 | D. | 10 mL 3 mol•L-1 Na2SO4溶液 |
17.下列有关化学用语表示正确的是( )
| A. | 羟基的电子式: | B. | 甲酸甲酯的最简式:C2H4O2 | ||
| C. | 苯甲醛的结构简式: | D. | 环戊烷的键线式: |
14.下列化学用语正确的是( )
| A. | 甲烷的电子式: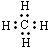 | |
| B. | 氟原子的结构示意图: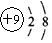 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 碳酸钠的电离方程式:Na2CO3=Na2++CO32- |
18.用下列实验装置进行相应实验,能达到实验目的是( )
| A. |  用图所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 | |
| B. |  用图所示装置蒸发掉CuCl2溶液中大部分水制得CuCl2•2H2O晶体 | |
| C. |  用图所示装置从乙酸和乙酸乙酯的混合液中分离得到纯净的乙酸乙酯 | |
| D. |  用图所示装置,用块状大理石与稀盐酸反应制取CO2气体 |
16.下列离子方程式书写正确的是( )
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 铝粉投入到 NaOH 溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | 铁粉与稀硫酸溶液反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Cl2 与烧碱溶液跟反应:Cl2+2OH-═Cl-+ClO-+H2O |
 不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.回答下列问题:
不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.回答下列问题: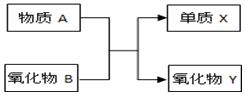 已知A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示(反应条件略):
已知A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示(反应条件略):