题目内容
15.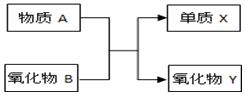 已知A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示(反应条件略):
已知A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示(反应条件略):试写出符合下列条件的化学方程式:
(1)若物质A为氧化物:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe;
(2)若A为金属单质,X均为非金属单质:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
分析 (1)物质A为氧化物,可知为两种氧化物反应生成单质、氧化物的反应,如CO还原氧化铁、CuO等;
(2)若A为金属单质,X均为非金属单质,可知为金属单质与氧化物发生的置换反应,且生成非金属单质,如Mg与二氧化碳反应.
解答 解:(1)物质A为氧化物,可知为两种氧化物反应生成单质、氧化物的反应,如CO还原氧化铁、CuO等,符合条件的反应如3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,
故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe;
(2)若A为金属单质,X均为非金属单质,可知为金属单质与氧化物发生的置换反应,且生成非金属单质,如Mg与二氧化碳反应,反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
6.下列离子方程式书写正确的是( )
| A. | 钠与水:2Na+2H2O═2Na++2 OH-+H2↑ | |
| B. | CaCO3与稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | FeCl3溶液与Fe反应:Fe3++Fe═2Fe2+ |
3.“绿色化学”是当今社会提出的一个新概念.在“绿色化学”工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%.利用以下各种化学反应类型的合成过程最符合绿色化学的是( )
| A. | 取代反应 | B. | 水解反应 | C. | 加聚反应 | D. | 缩聚反应 |
20.只有一种试剂可以一次性鉴别Na2CO3、MgCl2、NH4Cl三种溶液,这种试剂是( )
| A. | 盐酸 | B. | 氯化钡 | C. | 硝酸银溶液 | D. | 氢氧化纳 |
7.下列有关“核外电子的运动状态”的说法,错误的是( )
| A. | 一个原子轨道就是电子在原子核外的一个空间运动状态 | |
| B. | 电子云表示处于一定空间运动状态电子在核外空间的概率密度分布的描述 | |
| C. | 原子轨道伸展方向与能量大小是无关的 | |
| D. | 除s电子云外,其他空间运动状态的电子云也可以是球形的 |
4.在某温度和体积不变的密闭容器中,一定质量的C与2mol CO2发生反应:C+CO2=2CO,测得反应后气体压强是反应前气体压强的$\frac{3}{2}$倍,下列说法中正确的是( )
| A. | 反应后容器内的气体只有CO | |
| B. | 反应后生成的CO与反应前的CO2的物质的量之比为1:1 | |
| C. | 反应后生成的CO与反应前的CO2的分子数目之比为3:2 | |
| D. | 反应后容器内的气体与反应前的CO2所含的氧原子数目之比为1:2 |