题目内容
(2010?广东)HA为酸性略强与醋酸的一元弱酸,在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
分析:根据HA为一元弱酸,则在0.1mol?L-1 NaA溶液中利用盐类水解及电荷守恒来分析溶液中离子的关系.
解答:解:A、因HA为一元弱酸,则NaA溶液中A-+H20═HA+OH-,即溶液显碱性,则c(OH-)>c(H+),故A错误;
B、由溶液中A-+H20═HA+OH-,则c(OH-)>c(H+),但水解的程度很弱,则c(A-)>c(OH-)>c(H+),故B错误;
C、由电荷守恒可知,溶液中阳离子带的电荷总数等于阴离子带的电荷总数,则c(Na+)+c(H+)=c(A-)+c(OH-),故C错误;
D、由电荷守恒可知,溶液中阳离子带的电荷总数等于阴离子带的电荷总数,则c(Na+)+c(H+)=c(A-)+c(OH-),故D正确;
故选:D.
B、由溶液中A-+H20═HA+OH-,则c(OH-)>c(H+),但水解的程度很弱,则c(A-)>c(OH-)>c(H+),故B错误;
C、由电荷守恒可知,溶液中阳离子带的电荷总数等于阴离子带的电荷总数,则c(Na+)+c(H+)=c(A-)+c(OH-),故C错误;
D、由电荷守恒可知,溶液中阳离子带的电荷总数等于阴离子带的电荷总数,则c(Na+)+c(H+)=c(A-)+c(OH-),故D正确;
故选:D.
点评:本题考查溶液中离子的关系,正确利用水解来判断溶液的酸碱性是解答的关键,并注意溶液中水解的程度及利用电荷守恒来分析解答即可.

练习册系列答案
相关题目
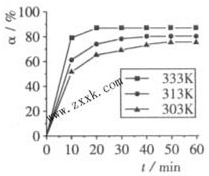 (2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛.
(2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛. B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出:
B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出: [B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)