题目内容
下列离子方程式书写正确的是( )
| A、实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
| B、铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+ |
| C、向AlCl3溶液中加入过量的NaOH 溶液:Al3++3OH-=Al(OH)3↓ |
| D、H2SO4溶液与NaOH溶液反应:OH-+H+=H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钙为难溶物,离子方程式中需要保留化学式;
B.铁与稀硝酸反应生成一氧化氮气体,不会生成氢气;
C.氢氧化钠过量,反应产物为偏铝酸根离子,不会生成氢氧化铝沉淀;
D.硫酸与氢氧化钠反应的实质为氢离子与氢氧根离子反应生成水.
B.铁与稀硝酸反应生成一氧化氮气体,不会生成氢气;
C.氢氧化钠过量,反应产物为偏铝酸根离子,不会生成氢氧化铝沉淀;
D.硫酸与氢氧化钠反应的实质为氢离子与氢氧根离子反应生成水.
解答:
解:A.实验室用大理石和稀盐酸制取CO2,碳酸钙应该保留化学式,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.稀硝酸为强氧化性的酸,铁与稀硝酸反应生成一氧化氮气体,不会生成氢气,故B错误;
C.向AlCl3溶液中加入过量的NaOH溶液,二者反应生成偏铝酸钠和水,正确的离子方程式为:Al3++4OH-=AlO2-+2H2O,故C错误;
D.H2SO4溶液与NaOH溶液反应生成可溶性硫酸钠和水,反应的离子方程式为:OH-+H+=H2O,故D正确;
故选D.
B.稀硝酸为强氧化性的酸,铁与稀硝酸反应生成一氧化氮气体,不会生成氢气,故B错误;
C.向AlCl3溶液中加入过量的NaOH溶液,二者反应生成偏铝酸钠和水,正确的离子方程式为:Al3++4OH-=AlO2-+2H2O,故C错误;
D.H2SO4溶液与NaOH溶液反应生成可溶性硫酸钠和水,反应的离子方程式为:OH-+H+=H2O,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,侧重对学生能力的培养和训练;注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
下列名言名句中隐含化学变化的是( )
| A、千里冰封,万里雪飘 |
| B、行到水穷处,坐看云起时 |
| C、野火烧不尽,春风吹又生 |
| D、只要功夫深,铁杵磨成针 |
下列说法中正确的是( )
| A、标准状况下,22.4L任何气体都含有约6.02×1023个分子 |
| B、含有6.02×1023个He原子的氦气在标准状况下的体积约为11.2L |
| C、常温常压下,11.2LCl2含有的Cl2为0.5mol |
| D、标准状况下,11.2LH2O含有的H2O为0.5mol |
原电池的主要功能是将化学能转化为( )
| A、热能 | B、光能 | C、核能 | D、电能 |
下列装置能构成原电池的是( )
A、 |
B、 |
C、 |
D、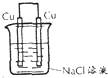 |
 观察如图所示的装置,回答下列问题:
观察如图所示的装置,回答下列问题: