题目内容
过氧化钙常用作种子消毒剂和鱼塘增氧剂,市售过氧化钙常带有数量不等的结晶水,通常还含有部分CaO.
(1)称取24.4g某过氧化钙样品,灼热时发生如下反应:2CaO2?xH2O
2CaO+O2↑+2xH2O.若得到的O2在标准状况下体积为2.24L,求该样品中CaO2的物质的量
(2)另取同一样品24.4g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g.试计算:
①样品中CaO的质量:
②样品中CaO2?xH2O的x值. .
(1)称取24.4g某过氧化钙样品,灼热时发生如下反应:2CaO2?xH2O
| △ |
(2)另取同一样品24.4g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g.试计算:
①样品中CaO的质量:
②样品中CaO2?xH2O的x值.
考点:化学方程式的有关计算
专题:计算题
分析:(1)O2在标准状况下体积为2.24L,n(O2)=
=0.1mol,由方程式计算CaO2的物质的量;
(2)Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g,n(Ca2+)=n(CaCO3)=
=0.25mol,结合M=
及相对分子质量的计算解答.
| 2.24L |
| 22.4L/mol |
(2)Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g,n(Ca2+)=n(CaCO3)=
| 25g |
| 100g/mol |
| m |
| n |
解答:
解:(1)O2在标准状况下体积为2.24L,n(O2)=
=0.1mol,
由2CaO2?xH2O
2CaO+O2↑+2xH2O可知,n(CaO2)=n(CaO2?xH2O)=2n(O2)=2×0.1mol=0.2mol,
故答案为:0.2mol;
(2)Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g,n(Ca2+)=n(CaCO3)=
=0.25mol,
①根据Ca元素守恒,可知:n(CaO)=0.25mol-0.2mol=0.05mol,
m(CaO)=0.05mol×56g/mol=2.8g,
故答案为:2.8g;
②样品中水的质量为:m(H2O)=24.4g-m(CaO2)-m(CaO)=24.4g-0.2mol×72g/mol-2.8g=7.2g,
n(H2O)=
=0.4mol,
x=
=2,
故答案为:2.
| 2.24L |
| 22.4L/mol |
由2CaO2?xH2O
| △ |
故答案为:0.2mol;
(2)Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO325g,n(Ca2+)=n(CaCO3)=
| 25g |
| 100g/mol |
①根据Ca元素守恒,可知:n(CaO)=0.25mol-0.2mol=0.05mol,
m(CaO)=0.05mol×56g/mol=2.8g,
故答案为:2.8g;
②样品中水的质量为:m(H2O)=24.4g-m(CaO2)-m(CaO)=24.4g-0.2mol×72g/mol-2.8g=7.2g,
n(H2O)=
| 7.2g |
| 18g/mol |
x=
| 0.4mol |
| 0.2mol |
故答案为:2.
点评:本题考查化学反应方程式的计算,注意根据反应的化学方程式,从质量守恒的角度计算.侧重分析能力及计算能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质属于电解质的是( )
| A、蔗糖 | B、铁单质 |
| C、KCl固体 | D、NaOH溶液 |
下列离子方程式书写正确的是( )
| A、实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
| B、铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+ |
| C、向AlCl3溶液中加入过量的NaOH 溶液:Al3++3OH-=Al(OH)3↓ |
| D、H2SO4溶液与NaOH溶液反应:OH-+H+=H2O |
下列对Na2CO3的分类,不正确的是( )
| A、Na2CO3是有机物 |
| B、Na2CO3是正盐 |
| C、Na2CO3是钠盐 |
| D、Na2CO3是碳酸盐 |
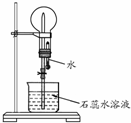 A是一种白色晶体,受热分解能生成B、C两种无色气体,C的水溶液与硝酸银溶液反应产生白色沉淀.A与浓NaOH溶液共热,放出无色气体B.若在圆底烧瓶中分别收集干燥的气体B和C,然后将收集满气体的烧瓶按如图所示装置组装,挤压滴管的胶头时,可以分别得到蓝色喷泉和红色喷泉.
A是一种白色晶体,受热分解能生成B、C两种无色气体,C的水溶液与硝酸银溶液反应产生白色沉淀.A与浓NaOH溶液共热,放出无色气体B.若在圆底烧瓶中分别收集干燥的气体B和C,然后将收集满气体的烧瓶按如图所示装置组装,挤压滴管的胶头时,可以分别得到蓝色喷泉和红色喷泉.