题目内容
8.0.5L1mol•L-1FeCl3溶液与0.2L1mol•L-1KCl溶液中的Cl-的数目之比为( )| A. | 5:2 | B. | 3:1 | C. | 15:2 | D. | 1:3 |
分析 根据溶液的浓度和化合物的组成判断两种溶液中离子浓度的关系,注意与溶液的体积无关,然后求出离子的物质的量,利用数目之比等于物质的量之比,由此分析解答.
解答 解:0.5L 1mol/L FeCl3溶液中c(Cl-)=3c(FeCl3)=3×1mol/L=3mol/L,n(Cl-)=0.5L×3mol/L=1.5mol;0.2L 1mol/L KCl溶液中c(Cl-)=c(KCl)=1mol/L,n(Cl-)=0.2L×1mol/L=0.2mol,所以数目之比等于1.5mol:0.2mol=15:2,故选:C.
点评 本题考查的是物质的量浓度的相关计算,利用数目之比等于物质的量之比,比较容易.

练习册系列答案
相关题目
18.乙酸分子结构中,含有的σ键和π键的个数分别是( )
| A. | 7、1 | B. | 6、2 | C. | 3、5 | D. | 4、4 |
19.1mol某饱和烷烃在氧气中充分燃烧,需要消耗氧气246.4L(标准状况下).它在光照的条件下与氯气反应能生成3种不同的一氯取代物.该烃的结构简式是( )
| A. | 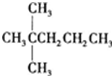 | B. | CH3CH2CH2CH2CH3 | C. | 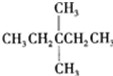 | D. | 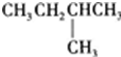 |
16.下列各组离子在给定条件下能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、SO32- | |
| B. | 有CO32-存在的溶液中:Na+、Mg2+、Ca2+、NO3- | |
| C. | 有MnO4-存在的酸性溶液中:Na+、Ba2+、Cl-、I- | |
| D. | 在c(H+):c(OH-)=1:10的水溶液中:Na+、SO42-、K+、S2- |
2.下列化学反应的产物中,存在同分异构体的是( )
| A. | CH3CH2CH2Br在碱性溶液中水解 | |
| B. | 甲苯在催化剂作用下与Cl2发生苯环上的取代反应 | |
| C. |  与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 | |
| D. |  在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
19.关于下列各组物质的叙述,正确的是( )
①H2N-CH2-COOH和H3C-CH2-NO2
②CH3COOH和HCOOCH3
③CH3CH2CHO 和 CH3COCH3
④CH3CH2CH2OH和CH3CH2OCH3
⑤2-甲基丙烷和丁烷
⑥CH3CH=CHCH2CH3和CH3CH2CH2CH=CH2
⑦CH3(CH2)4CH3 和 CH3CH(CH3)CH2CH3.
①H2N-CH2-COOH和H3C-CH2-NO2
②CH3COOH和HCOOCH3
③CH3CH2CHO 和 CH3COCH3
④CH3CH2CH2OH和CH3CH2OCH3
⑤2-甲基丙烷和丁烷
⑥CH3CH=CHCH2CH3和CH3CH2CH2CH=CH2
⑦CH3(CH2)4CH3 和 CH3CH(CH3)CH2CH3.
| A. | ①②③④⑤⑥⑦都是同分异构体 | B. | ⑥是官能团异构类型 | ||
| C. | ⑦是碳链异构类型 | D. | ①②③④是官能团异构类型 |
20.下列说法正确的是( )
| A. | 相对分子质量相同的物质是同种物质 | |
| B. | 分子式相同的不同有有机物一定是同分异构体 | |
| C. | 具有同一通式的物质属于同系物 | |
| D. | 分子中含有碳和氢的化合物是烃类 |