题目内容
有A、B、C三种短周期元素.A原子的最外层电子数是次外层电子数的三倍,而B原子的次外层电子数是最外层电子数的四倍,C原子的K、L层电子数之和比K、M层电子数之和多1个.回答下列问题:
(1)写出A、B、C的元素符号:A是 ,B是 ,C是 .
(2)C元素位于周期表中第 周期第 族.
(3)B离子的结构示意图是 .B、C两元素形成的化合物的电子式是 .
(1)写出A、B、C的元素符号:A是
(2)C元素位于周期表中第
(3)B离子的结构示意图是
考点:位置结构性质的相互关系应用
专题:
分析:短周期元素A最外层电子数是次外层的三倍,次外层电子数为2,最外层电子数为6,即A为O元素;B原子的次外层电子数是最外层电子数的四倍,则次外层电子数为8,最外层电子数为2,即B为Mg元素;C原子的K、L层电子数之和比K、M层电子数之和多1个,则L层电子数为8,M层电子数为7,即C为Cl元素,据此解答.
解答:
解:短A原子的最外层电子数是次外层电子数的三倍,次外层电子数为2,最外层电子数为6,即A为O元素;B原子的次外层电子数是最外层电子数的四倍,则次外层电子数为8,最外层电子数为2,即B为Mg元素;C原子的K、L层电子数之和比K、M层电子数之和多1个,则L层电子数为8,M层电子数为7,即C为Cl元素,
(1)由上分析,A为O,B为Mg,C为Cl,故答案为:O;Mg:Cl;
(2)C为Cl,为第三周期第ⅤⅡA族,故答案为:三;ⅤⅡA;
(3)B为Mg,镁离子结构示意图为 ,Mg与Cl形成的化合物为MgCl2,电子式为
,Mg与Cl形成的化合物为MgCl2,电子式为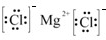 ,
,
故答案为: ;
;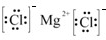 .
.
(1)由上分析,A为O,B为Mg,C为Cl,故答案为:O;Mg:Cl;
(2)C为Cl,为第三周期第ⅤⅡA族,故答案为:三;ⅤⅡA;
(3)B为Mg,镁离子结构示意图为
 ,Mg与Cl形成的化合物为MgCl2,电子式为
,Mg与Cl形成的化合物为MgCl2,电子式为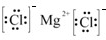 ,
,故答案为:
 ;
;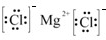 .
.
点评:本题主要考查了根据原子核外各层电子数的关系,确定元素的种类,难度不大,解题时要熟悉常见元素的核外电子排布,注意规范书写结构示意图.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、HCO3-的水解:HCO3-+H2O?CO32-+H3O+ |
| B、Na2S的水解:S2-+2H2O?H2S+2OH- |
| C、Fe3+的检验:Fe3++3SCN-?Fe(SCN)3↓ |
| D、Cu(OH)2溶于氨水形成深蓝色溶液:Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O |
下列说法中,正确的是( )
①同种元素的原子性质一定相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥金属导电和电解质溶液的导电都是物理变化.
①同种元素的原子性质一定相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥金属导电和电解质溶液的导电都是物理变化.
| A、①④⑥ | B、②③⑤ |
| C、②④⑤ | D、①③⑥ |
下列有关叙述正确的是:①不同种元素形成的共价分子中只存在极性键②在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+)③离子化合物的熔点一定比共价化合物的熔点高④乙醇易溶于水的主要原因是乙醇分子与水分子间能形成氢键( )
| A、①②③ | B、②③ | C、②④ | D、全部 |
下列分子中所有原子都满足最外层8电子结构的是( )
| A、二氟化氙 | B、三氯化磷 |
| C、六氟化硫 | D、三氟化硼 |
1977年在印度洋东南部马德里斯的一个海湾里,一阵飓风过后,海面的巨浪上竟燃烧着熊熊大火.海水会燃烧的原因是( )
| A、时速达280公里的飓风与海水发生剧烈摩擦,产生的巨大热能使水分子分解,引起氢气燃烧 |
| B、飓风使海水分子运动速度加快,产生的热能使海水中植物燃烧 |
| C、海面上漂浮的油层被氧化而燃烧 |
| D、以上叙述都正确 |
 全氮型超高能材料是指能量比常规炸药至少高一个数量级的新型高能物质,它最突出的特性是分子中蕴含有巨大的能量.
全氮型超高能材料是指能量比常规炸药至少高一个数量级的新型高能物质,它最突出的特性是分子中蕴含有巨大的能量.


 是E的最简单的同系物,试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件)
是E的最简单的同系物,试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件)