题目内容
Na2S2O3可作为脱氧剂,已知25.0mL0.100mol?L-1Na2S2O3溶液恰好与224mL(标准状况下)Cl2完全反应,则S2O32-将转化成( )
| A、S2- |
| B、S |
| C、SO32- |
| D、SO42- |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等列式计算.
解答:
解:n(Na2S2O3)=0.025L×0.100mol/L=0.0025mol,n(Cl2)=
=0.01mol,
设S2O32-被氧化后的S元素的化合价为n,
根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等,则
0.0025×2×(n-2)mol=2×0.01mol
n=6,
故选D.
| 0.224L |
| 22.4L/mol |
设S2O32-被氧化后的S元素的化合价为n,
根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等,则
0.0025×2×(n-2)mol=2×0.01mol
n=6,
故选D.
点评:本题考查氧化还原反应的计算,题目难度不大,注意从氧化剂、还原剂得失电子数目相等的角度解答.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
下列分子中的中心原子采取sp2杂化的是( )
①C6H6 ②C2H2 ③C2H4 ④C3H8 ⑤CO2 ⑥BeCl2⑦SO3 ⑧BF3.
①C6H6 ②C2H2 ③C2H4 ④C3H8 ⑤CO2 ⑥BeCl2⑦SO3 ⑧BF3.
| A、①②⑥⑦ | B、③⑤⑦⑧ |
| C、①③⑦⑧ | D、③⑤⑥⑦ |
已知同温度下,三种酸的电离平衡常数的大小关系为Ka(HX)>Ka(HY)>Ka(HZ),则物质的量浓度相同的三种盐NaX、NaY和NaZ溶液pH由大到小的顺序是( )
| A、NaX NaY NaZ |
| B、NaX NaZ NaY |
| C、NaY NaZ NaX |
| D、NaZ NaY NaX |
下列物质加入水中,显著放热的是( )
| A、二氧化硅 |
| B、生石灰 |
| C、无水乙醇 |
| D、固体NH4NO3 |
按如图所示装置,以石墨为电极电解氯化铜溶液,正确的是( )


| A、阴极为A |
| B、阳极电极反应式Cu2++2e-=Cu |
| C、在B极观察到有气泡,产生的气体能使湿润的淀粉-KI变蓝 |
| D、溶液中Cu2+移向B极 |
下列物质中,在标准状况下体积最大的是( )
| A、48g O2 |
| B、71g Cl2 |
| C、28g N2 |
| D、1000g H2O |
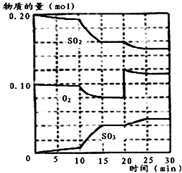 已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题:
已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题: