题目内容
 (2011?湖南二模)[化学一选修化学与技术]
(2011?湖南二模)[化学一选修化学与技术]纯碱(Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
【实验室制备纯碱】
(1)将饱和NaCl溶液倒入烧杯中加热,控制温度为30?350C
(2)搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟
(3)静置、过滤得NaHCO3晶体
(4)用少量蒸馏水洗涤、抽干
(5)将所得固体转人蒸发皿中灼烧得Na2CO3固体
问题:①反应将温度需控制在30?35曟,通常采取的加热方法为
水浴加热
水浴加热
;控制该温度的原因是温度过高时碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率
温度过高时碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率
.②静置后只析出NaHCO3晶体的原因是
相同温度下,碳酸氢钠的溶解度小
相同温度下,碳酸氢钠的溶解度小
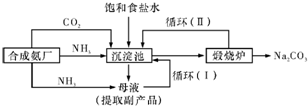
.【工业制备纯碱】
③沉淀池中反应的离子方程式为
NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓
NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓
;④循环(I)、循环(II)中物质的化学式分别为
NaCl、CO2
NaCl、CO2
.两种制备纯碱的方法中,共同涉及的化学反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,
2NaHCO3
Na2CO3+H2O+CO2↑
2NaHCO3
| ||
NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,
2NaHCO3
Na2CO3+H2O+CO2↑
.2NaHCO3
| ||
分析:①水浴加热的定义是把要加热的物质放在水中,通过给水加热达到给物质加热的效果.水浴加热的优点是避免了直接加热造成的过度剧烈与温度的不可控性,可以平稳地加热.水浴加热的缺点是加热温度最高只能达到100度.碳酸氢铵在低于30℃时分解较少,高于40℃时剧烈分解碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率.所以反应温度需控制在30?35℃,用水浴加热较好;
②碳酸氢钠和碳酸氢铵的溶解度的考察,碳酸氢铵在20℃时溶解度为21.7 g,碳酸氢钠20℃时溶解度为9.6 g,30℃时为11.1 g,相同温度下,碳酸氢钠的溶解度更小,在溶液中更易析出;
③侯氏制碱法中沉淀池中化学为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,改写为离子方程式时氯化钠和氯化铵可以拆开,碳酸氢钠不可以拆开,即为NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓;④在母液中加入盐酸,生成氯化钠,通过循环Ⅰ供循环使用;煅烧碳酸氢钠释放出的二氧化碳通过循环Ⅱ重新进入沉淀池进行循环利用.侯氏制碱法(联合制碱法)的反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,氨碱法(索氏制碱法)的方程式为 NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,得到的碳酸氢钠受热分解生成碳酸钠,2NaHCO3
Na2CO3+H2O+CO2↑.故共同的方程式为①NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,②2NaHCO3
Na2CO3+H2O+CO2↑.
②碳酸氢钠和碳酸氢铵的溶解度的考察,碳酸氢铵在20℃时溶解度为21.7 g,碳酸氢钠20℃时溶解度为9.6 g,30℃时为11.1 g,相同温度下,碳酸氢钠的溶解度更小,在溶液中更易析出;
③侯氏制碱法中沉淀池中化学为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,改写为离子方程式时氯化钠和氯化铵可以拆开,碳酸氢钠不可以拆开,即为NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓;④在母液中加入盐酸,生成氯化钠,通过循环Ⅰ供循环使用;煅烧碳酸氢钠释放出的二氧化碳通过循环Ⅱ重新进入沉淀池进行循环利用.侯氏制碱法(联合制碱法)的反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,氨碱法(索氏制碱法)的方程式为 NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,得到的碳酸氢钠受热分解生成碳酸钠,2NaHCO3
| ||
| ||
解答:解:①水浴加热是把要加热的物质放在水中,通过给水加热达到给物质加热的效果.一般都是把要反应的物质放在试管中,再把试管放在装有水的烧杯中,再在烧杯中插一根温度计,可以控制反应温度.水浴加热的优点是避免了直接加热造成的过度剧烈与温度的不可控性,可以平稳地加热,许多反应需要严格的温度控制,就需要水浴加热.水浴加热的缺点是加热温度最高只能达到100度.反应将温度需控制在30?35℃,用水浴加热较好.碳酸氢铵在低于30℃时分解较少,高于40℃时剧烈分解碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率.
故答案为:水浴加热;温度过高时碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率;
②碳酸氢铵在20℃时溶解度为21.7 g,碳酸氢钠20℃时溶解度为9.6 g,30℃时为11.1 g,相同温度下,碳酸氢钠的溶解度更小,更易析出.
故答案为:相同温度下,碳酸氢钠的溶解度小;
③侯氏制碱法中沉淀池中化学反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,改写为离子方程式即为
NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓.
故答案为:NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓;
④循环Ⅰ是在母液中加入盐酸,生成氯化钠,供循环使用;循环Ⅱ是煅烧碳酸氢钠释放出的二氧化碳重新进入沉淀池进行循环利用.侯氏制碱法(联合制碱法)的反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,氨碱法(索氏制碱法)的方程式为 NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,得到的碳酸氢钠受热分解生成碳酸钠,2NaHCO3
Na2CO3+H2O+CO2↑.
故答案为:NaCl、CO2;NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,2NaHCO3
Na2CO3+H2O+CO2↑.
故答案为:水浴加热;温度过高时碳酸氢铵受热分解剧烈,温度太低又减慢了化学反应的速率;
②碳酸氢铵在20℃时溶解度为21.7 g,碳酸氢钠20℃时溶解度为9.6 g,30℃时为11.1 g,相同温度下,碳酸氢钠的溶解度更小,更易析出.
故答案为:相同温度下,碳酸氢钠的溶解度小;
③侯氏制碱法中沉淀池中化学反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,改写为离子方程式即为
NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓.
故答案为:NH3+CO2+H2O+Na++Cl-=NH4++Cl-+NaHCO3↓;
④循环Ⅰ是在母液中加入盐酸,生成氯化钠,供循环使用;循环Ⅱ是煅烧碳酸氢钠释放出的二氧化碳重新进入沉淀池进行循环利用.侯氏制碱法(联合制碱法)的反应方程式为NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,氨碱法(索氏制碱法)的方程式为 NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,得到的碳酸氢钠受热分解生成碳酸钠,2NaHCO3
| ||
故答案为:NaCl、CO2;NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,2NaHCO3
| ||
点评:本题考查了侯氏制碱法的基本流程、反应的方程式、反应条件的控制、原料的循环利用,将化学反应方程式转化为离子反应方程式时注意碳酸氢钠不要写成离子的形式,制碱方法的两种常见方法为侯氏制碱法和索氏制碱法,反应的方程式和工艺流程等方面为常考查的热点.

练习册系列答案
相关题目

 (2011?湖南二模)2011年3月3日晚联合国教科文组织在其巴黎总部举行世界杰出女科学家奖颁奖仪式.香港大学无机化学教授任咏华,她因在发光材料和太阳能创新技术方面取得突出成就而获奖.她主要研究无机发光材料,“魔棒”是一种有机发光材料,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如下.下列有关说法正确的是( )
(2011?湖南二模)2011年3月3日晚联合国教科文组织在其巴黎总部举行世界杰出女科学家奖颁奖仪式.香港大学无机化学教授任咏华,她因在发光材料和太阳能创新技术方面取得突出成就而获奖.她主要研究无机发光材料,“魔棒”是一种有机发光材料,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如下.下列有关说法正确的是( )