题目内容
10.能发生离子反应,但不会产生沉淀的是( )| A. | 澄清石灰水中通入CO2 | B. | NaHCO3溶液中滴加NaOH溶液 | ||
| C. | MgSO4溶液中滴加NaOH溶液 | D. | 氯化钠溶液中加硝酸银溶液 |
分析 离子之间结合生成沉淀、气体、水等,均可发生离子反应,结合不生成沉淀来解答.
解答 解:A.反应生成碳酸钙沉淀,故A不选;
B.反应生成碳酸钠和水,没有沉淀,故B选;
C.反应生成氢氧化镁沉淀,故C不选;
D.反应生成AgCl沉淀,故D不选;
故选B.
点评 本题考查离子反应,为基础性习题,把握复分解反应的条件及常见离子之间的反应为解答的关键,注意常见的难溶物判断,题目较简单.

练习册系列答案
相关题目
20.阿司匹林是一种常用的解热镇痛药,其结构如图,有关推断不正确的是( )
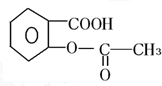

| A. | 可以与碱发生反应 | B. | 可以发生水解反应 | ||
| C. | 该物质易溶于水 | D. | 可以发生酯化反应 |
1.现有失去标签的氯化镁、碳酸钠、硫酸氢钠、氢氧化钡四种无色溶液,为了确定四种溶液各是什么,将它们随意编号A、B、C、D后进行实验,其实验现象如表
根据实验现象,按要求回答:
(1)写出各物质的化学式ABa(OH)2、BNaHSO4、CNa2CO3、DMgCl2
(2)写出实验中反应②的离子方程式2H++CO32-=CO2↑+H2O向A中滴加少量的B的离子方程式H++SO42-+OH-+Ba2+=BaSO4↓+H2O,继续滴加的离子方程式H++OH-=H2O.
| 反应编号 | 反应物质 | 有关现象 |
| ① | A+B | 有沉淀生成 |
| ② | B+C | 有气体放出 |
| ③ | C+D | 有沉淀生成 |
| ④ | B+D | 无明显现象 |
| ⑤ | A+D | 有沉淀生成 |
(1)写出各物质的化学式ABa(OH)2、BNaHSO4、CNa2CO3、DMgCl2
(2)写出实验中反应②的离子方程式2H++CO32-=CO2↑+H2O向A中滴加少量的B的离子方程式H++SO42-+OH-+Ba2+=BaSO4↓+H2O,继续滴加的离子方程式H++OH-=H2O.
18.下列说法不正确的是( )
| A. | 过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 | |
| B. | 乙醇和水可以任意比互溶,主要是因为乙醇和水分子间能形成氢键 | |
| C. | 硫酸钡、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 | |
| D. | 煤的气化、液化和干馏均属于化学变化 |
5.某元素一价阴离子的核外有18个电子,质量数为35,该微粒符号可表示为( )
| A. | ${\;}_{18}^{35}$Cl- | B. | ${\;}_{17}^{35}$Cl | C. | ${\;}_{19}^{35}$Cl- | D. | ${\;}_{17}^{35}$Cl- |
19.下列有关氧族元素的叙述中,正确的是( )
| A. | 都能生成+6价化合物 | B. | 原子的最外层电子数都是6 | ||
| C. | 都能生成稳定的氢化物 | D. | 单质在通常情况下均为固体 |
20.常温下,下列溶液的离子浓度关系式正确的是( )
| A. | pH=6的H2S溶液中,c(H+)=c(HS-)=1×10-6mol•L-1 | |
| B. | pH=a的醋酸溶液,稀释10倍后,其pH=b,则b=a+1 | |
| C. | pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液pH<7:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | pH相同的①CH3COONa、②Na2CO3、③NaClO三种溶液的c(Na+):①<②<③ |
 如图为某原电池装置:
如图为某原电池装置: