题目内容
燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于CO燃料电池的说法中不正确的是( )
| A、燃料电池是把化学能转化为电能的装置 | ||
B、负极的电极反应式为CO+4OH--2e-═CO
| ||
| C、随着反应的进行,电解质溶液的pH保持不变 | ||
| D、通入氧气的一极发生还原反应,通入CO的一极发生氧化反应 |
考点:化学电源新型电池
专题:电化学专题
分析:燃料电池是燃料跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,燃料气体通入的是原电池的负极失电子发生氧化反应,氧气通入的是正极发生还原反应.
解答:
解:燃料电池是燃料跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,燃料气体通入的是原电池的负极失电子发生氧化反应,氧气通入的是正极发生还原反应;
A、燃料电池是将化学能装化为电能的装置,故A正确;
B、正极反应为O2+2H2O+4e-=4OH-;总化学方程式为:CH4+2O2+2OH-=CO32-+3H2O;总反应减去正极反应得到负极的电极反应式为:CO+4OH--2e-═CO32-+2H2O,故B正确;
C、随着不断放电,原电池反应中反应生成水,氢氧根离子浓度减小,电解质溶液的pH减小,故C错误;
D、通入氧气的一极发生还原反应,通入CO的一极发生氧化反应,故D正确.
故选C.
A、燃料电池是将化学能装化为电能的装置,故A正确;
B、正极反应为O2+2H2O+4e-=4OH-;总化学方程式为:CH4+2O2+2OH-=CO32-+3H2O;总反应减去正极反应得到负极的电极反应式为:CO+4OH--2e-═CO32-+2H2O,故B正确;
C、随着不断放电,原电池反应中反应生成水,氢氧根离子浓度减小,电解质溶液的pH减小,故C错误;
D、通入氧气的一极发生还原反应,通入CO的一极发生氧化反应,故D正确.
故选C.
点评:本题考查了化学新型电源电池的应用,主要是电极名称,电极反应,电极反应的判断和应用,题目难度中等.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在.以Al-H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极).下列说法不正确的是( )

| A、燃料电池的总反应为:2Al+3HO2-=2AlO2-+OH-+H2O |
| B、电极b是正极,且反应后该电极区pH增大 |
| C、电解过程中,电子的流向由a→b→c→d. |
| D、电解时,Al消耗2.7g,则产生氮气标准状况下为1.12L |
混合物:①汽油和水;②苯和四氯化碳;③氯化钠和单质溴的水溶液,若分离以上各混合物中的两种成分,正确的分离方法依次是( )
| A、分液、蒸馏、萃取 |
| B、萃取、蒸馏、分液 |
| C、分液、萃取、蒸馏 |
| D、蒸馏、萃取、分液 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+11.9kJ?mol-1可知,金刚石比石墨稳定 |
| C、在25℃,101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1 |
| D、H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量等于57.3kJ |
下列说法正确的是( )
| A、pH=0的溶液不存在 |
| B、中性溶液的pH不一定等于7 |
| C、使用广泛pH试纸测得某溶液的pH=3.5 |
| D、酸或碱溶液在稀释时,溶液的pH均减小 |
设NA为阿佛伽德罗常数,下列叙述正确的是( )
| A、28克氮气所含的氮原子数为2NA |
| B、1L1mol/L的盐酸中含有氯化氢分子为NA |
| C、标况下,11.2L水中所含的分子数为0.5NA |
| D、铁与盐酸中的反应,1mol铁失去的电子数为3NA |
“原子经济性”是“绿色化学”重要内涵.它主张在化学转化获取新物质的过程中充分利用每个原子,这样既能够充分利用资源,又能够防止污染.从“原子经济性”的角度考虑,以下转化最合理的是( )
| A、消除制硝酸工业尾气的氮氧化物污染:NO2+NO+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O | ||||
B、制备Cu(NO3)2:2Cu+O2
| ||||
C、利用二氧化碳制造全降解塑料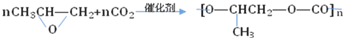 | ||||
D、用铜与浓硫酸共热制硫酸铜:Cu+2H2SO4(浓)
|
已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g?mL-1,要从水与丙酮的混合物里将丙酮分离出来,下列方法中最合理的是( )
| A、分液 | B、蒸馏 | C、过滤 | D、蒸发 |