题目内容
8.用100mL物质的量浓度为0.5mol/L NaHCO3溶液,可配制0.01mol/L NaHCO3多少毫升?分析 根据溶液稀释前后溶质的物质的量保持不变来回答.
解答 解:溶液稀释前后溶质的物质的量保持不变,设可以配制0.01mol/L NaHCO3的体积为V,则100mL×0.5mol/L=VmL×0.01mol/L,解得V=5000mL,答:可配制0.01mol/L NaHCO35000毫升.
点评 本题考查物质的量浓度的计算,为高频考点,把握质量、物质的量、浓度的关系为解答的关键,侧重计算能力的考查,题目难度不.

练习册系列答案
相关题目
1.某烯烃的结构简式为 ,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯.下列对四位同学的命名判断正确的是( )
,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯.下列对四位同学的命名判断正确的是( )
 ,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯.下列对四位同学的命名判断正确的是( )
,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯.下列对四位同学的命名判断正确的是( )| A. | 甲的命名主链选择是错误的 | B. | 乙的命名正确 | ||
| C. | 丙的命名主链选择是正确的 | D. | 丁的命名正确 |
19.下列关于元素周期表的说法正确的是( )
| A. | 短周期有一共有3个周期,22种元素 | |
| B. | 元素周期表共有七个周期,十八个族 | |
| C. | 科学研究时,常在周期表金属和非金属的分界线的位置寻找半导体材料 | |
| D. | 元素周期表中每一周期的元素是按照相对原子质量从小到大依次排列 |
3.下列说法正确的是( )
| A. | Na2O、Na2O2、CaO均属于碱性氧化物 | |
| B. | H2和HD属于同素异形体 | |
| C. | 蓝色的硫酸铜晶体遇到浓硫酸变白色属于化学变化 | |
| D. | 胶体带电,所以胶体具有电泳的性质 |
13.能在溶液中大量共存的一组离子是( )
| A. | Ag+、SO42-、Cl- | B. | Fe2+、H+、NO3- | ||
| C. | K+、Na+、NO3- | D. | Mg2+、SO42-、CO32- |
20.某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为( )
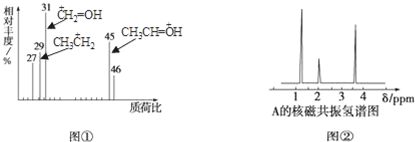

| A. | CH3CH2OH | B. | CH3CHO | C. | CH3OCH3 | D. | CH3CH2COOH |
17.焙烧FeS的反应为 4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2,关于该反应的叙述正确的是( )
| A. | 该反应属于置换反应 | |
| B. | SO2既是氧化产物,又是还原产物 | |
| C. | 每生成1 mol Fe2O3,转移14mol电子 | |
| D. | 若生成2.24LSO2,则生成8g Fe2O3 |