题目内容
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 甲烷(乙烯) | 溴水 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 乙醇(乙酸) | 无 | 分液 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:A.溴易溶于苯;
B.乙烯与溴水反应,而甲烷不能;
C.二者均与NaOH溶液反应;
D.乙醇、乙酸不分层.
B.乙烯与溴水反应,而甲烷不能;
C.二者均与NaOH溶液反应;
D.乙醇、乙酸不分层.
解答:
解:A.溴易溶于苯,且生成的三溴苯酚也溶于苯,引入新杂质,不符合除杂原则,故A错误;
B.乙烯与溴水反应,而甲烷不能,则利用溴水和洗气法可除杂,故B正确;
C.二者均与NaOH溶液反应,应利用饱和碳酸钠溶液除杂,故C错误;
D.乙醇、乙酸不分层,应利用蒸馏原理除杂,故D错误;
故选B.
B.乙烯与溴水反应,而甲烷不能,则利用溴水和洗气法可除杂,故B正确;
C.二者均与NaOH溶液反应,应利用饱和碳酸钠溶液除杂,故C错误;
D.乙醇、乙酸不分层,应利用蒸馏原理除杂,故D错误;
故选B.
点评:本题考查物质分离、提纯的基本方法和选择,为高频考点,把握物质的性质及常见的混合物分离方法为解答的关键,注意物质性质及分离原理,题目难度不大.

练习册系列答案
相关题目
Fe与稀H2SO4反应制取氢气,下列措施一定能使生成氢气的速率加快的是( )
| A、增加铁的量 | B、增大硫酸的浓度 |
| C、加热 | D、增大压强 |
氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A、都不稳定 |
| B、能透过滤纸 |
| C、分散质粒子直径在1 nm~100 nm之间 |
| D、呈红褐色 |
如图,下列叙述正确的是( )
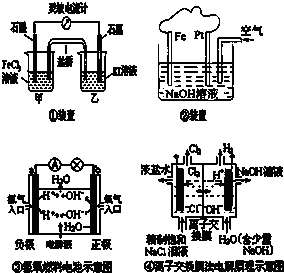

| A、①装置的总反应为2Fe3+2I-═2Fe2++I2 |
| B、②装置中Fe为阴极,电极反应为 Fe-2e-+2OH-═Fe(OH)2 |
| C、③装置中外电路电子由b极流向a极 |
| D、④装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
根据阿伏加德罗定律,下列叙述中正确的是( )
| A、同温同压下两种气体的体积之比等于摩尔质量之比 |
| B、同温同压下两种气体的质量之比等于物质的量之比 |
| C、同温同压下两种气体的物质的量之比等于密度之比 |
| D、同温同压下两种气体的摩尔质量之比等于密度之比 |
下列离子方程式中,正确的是( )
| A、稀硫酸与Ba(OH)2溶液混合:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、实验室制CO2:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、铁与稀硫酸反应 2 Fe+6H+=2Fe3++3H2↑ |
下列物质反应时,不会产生H2 的是 ( )
| A、Al+盐酸 |
| B、Al+HNO3(浓 常温) |
| C、Al+NaOH溶液 |
| D、Al+热H2O |