题目内容
5.某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原硝酸的物质的量之比为3:2时,还原产物可能是( )| A. | NO2 | B. | NO | C. | N2O | D. | N2 |
分析 在氧化还原反应中氧化剂得到的电子数等于还原剂失去的电子数,金属反应后化合价可能为+1、+2、+3价,根据转移电子数相等确定还原产物中N元素的化合价,从而确定还原产物.
解答 解:假设金属元素化合价由0价变为+1价,设还原产物中N元素化合价为x,根据转移电子相等得:3×(1-0)=2×(5-x),x=3.5,不存在;
假设金属元素化合价由0价变为+2价,设还原产物中N元素化合价为y,根据转移电子相等得3×(2-0)=2×(5-y),y=2;
假设金属元素化合价由0价变为+3价,设还原产物中N元素化合价为z,根据转移电子相等得3×(3-0)=2×(5-z),z=0.5;
根据分析可知,还原产物中N的化合价为+2价,
A.NO2中N元素化合价为+4价,不符合,故A错误;
B.NO中N元素化合价为+2价,符合,故B正确;
C.N2O中N元素化合价为+1,不符合,故C错误;
D.N2中N元素化合价为0价,不符合,故D错误;
故选B.
点评 本题考查氧化还原反应计算,侧重考查学生发散思维能力及计算能力,利用转移电子守恒解答即可,注意金属单质未知,其化合价需要讨论,为易错点.

练习册系列答案
相关题目
15.如图是从元素周期表中截取下来的,A、B、C为短周期主族元素,下列说法中正确的是( )
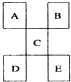

| A. | D一定足金属元素,其金属性比C强 | |
| B. | C的最高价氧化物水化物显强酸性 | |
| C. | E的原子序数一定是A的5倍,且原予半径比A大 | |
| D. | B的氢化物是以分子形式存在,且分子间存在氢键 |
16.下列第三周期的元素中,原子半径最小的是( )
| A. | S | B. | F | C. | Na | D. | O |
13.有A、B、C、D四种金属,投入水中只有C反应放出氢气,将A投入B的盐溶液中可置换出金属B,D的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )
| A. | A>B>C>D | B. | D>B>A>C | C. | B>D>A>C | D. | C>D>A>B |
20.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 医学上,血液透析是利用了胶体的渗析原理 | |
| B. | 碳酸氢钠可用于制备纯碱,作治疗胃酸过多的药物及食品发酵剂 | |
| C. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 | |
| D. | 铜的金属性比铝弱,可以用铜罐贮运浓硝酸 |
17.将 E 和 F 加入密闭容器中,在一定条件下发生反应:2E(g)+F(s)?G(g).忽略固体体积,平衡时 E的体积分数(%)随温度和压强的变化如下表所示.下列推断不正确的是( )
 | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A. | 915℃,2.0 MPa 时 E 的转化率为 60% | |
| B. | K(810℃)>K(1000℃) | |
| C. | 该反应可在较低温度下自发进行 | |
| D. | e>d |
14.下表列出了十种元素在周期表中的位置,用化学用语回答下列问题:
请回答:
(1)在这些元素中,化学性质最不活泼的是Ar(填元素符号).与其具有相同的电子层结构的是表中②和⑨的简单离子,它们的离子结构示意图为 、
、 .
.
(2)形成化合物种类最多的元素是C(填元素符号),其稳定氧化物的结构式为O=C=O.
(3)⑤、⑥、⑦、⑧四种元素所对应的气态氢化物最稳定的是H2O(填化学式).
(4)以上第三周期元素中的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式),二者发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(5)①、②、③的原子半径由大到小的顺序为K>Na>Mg(填元素符号).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑦ | ||||||
| 3 | ① | ③ | ④ | ⑥ | ⑧ | ⑨ | ⑩ | |
| 4 | ② |
(1)在这些元素中,化学性质最不活泼的是Ar(填元素符号).与其具有相同的电子层结构的是表中②和⑨的简单离子,它们的离子结构示意图为
 、
、 .
.(2)形成化合物种类最多的元素是C(填元素符号),其稳定氧化物的结构式为O=C=O.
(3)⑤、⑥、⑦、⑧四种元素所对应的气态氢化物最稳定的是H2O(填化学式).
(4)以上第三周期元素中的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式),二者发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(5)①、②、③的原子半径由大到小的顺序为K>Na>Mg(填元素符号).
15.有关合金的说法不正确的是( )
| A. | 合金的熔点比它的各成分金属的熔点低 | |
| B. | 合金一定是金属熔合而成的物质 | |
| C. | 合金的硬度和强度一般比纯金属大 | |
| D. | 硬铝、黄铜、钢等均为合金 |