题目内容
关于物质的用途说法错误的是( )
| A、二氧化硅用于制造光导纤维 |
| B、聚氯乙烯塑料(PVC)可制成薄膜做食品包装材料 |
| C、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| D、铝合金用于制造门窗 |
考点:硅和二氧化硅,金属与合金在性能上的主要差异,镁、铝的重要化合物,有机高分子化合物的结构和性质
专题:化学应用
分析:A.二氧化硅为光导纤维的主要原料;
B.聚氯乙烯塑料不能用作食品包装材料;
C.Si3N4、Al2O3熔点高;
D.铝合金熔点高、硬度大.
B.聚氯乙烯塑料不能用作食品包装材料;
C.Si3N4、Al2O3熔点高;
D.铝合金熔点高、硬度大.
解答:
解:A.二氧化硅具有较强的折光性,为光导纤维的主要原料,故A正确;
B.聚氯乙烯塑料在加热时释放出有害物质,不利于人体健康,不能用作食品包装材料,故B错误;
C.Si3N4、Al2O3熔点高,可用于制作高温结构陶瓷制品,故C正确;
D.铝合金熔点高、硬度大,可用于制造门窗,故D正确.
故选B.
B.聚氯乙烯塑料在加热时释放出有害物质,不利于人体健康,不能用作食品包装材料,故B错误;
C.Si3N4、Al2O3熔点高,可用于制作高温结构陶瓷制品,故C正确;
D.铝合金熔点高、硬度大,可用于制造门窗,故D正确.
故选B.
点评:本题考查较为综合,为高考常见题型,侧重于元素化合物知识与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
下列装置中(杯中均盛海水)铁腐蚀最快的是( )
A、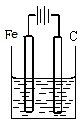 |
B、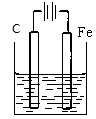 |
C、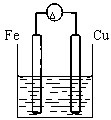 |
D、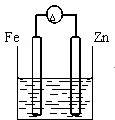 |
下列关于电解质溶液的叙述正确的是( )
| A、室温下,pH=3的氢氟酸加水稀释后,电离常数Ka(HF)和pH均减小 | ||
| B、室温下,将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | ||
C、向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
| ||
| D、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色 |
下列物质不能发生水解反应的是( )
| A、蛋白质 | B、蔗糖 | C、油脂 | D、烷烃 |
已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2).为了提高氯水中HClO的浓度,可行的是( )
| A、通入HCl(g) |
| B、加入NaHCO3(s) |
| C、加入H2O |
| D、加入NaOH(s) |
下列说法中错误的是( )
| A、CO燃烧是放热反应 |
| B、浓硫酸在常温下能够使铁、铝等金属钝化 |
| C、CaO与H2O反应是吸热反应 |
| D、Na与NaCl在灼烧时火焰颜色相同 |
常温下,对于①0.1mol/L CH3COOH溶液 ②pH=1HCl溶液 ③pH=13的NaOH溶液 ④0.1mol/L CH3COONa溶液,下列说法正确的是( )
| A、①和②分别稀释100倍后的pH:②>① | ||
| B、水电离出的c(OH-):④>③>①>② | ||
C、①和③混合后溶液呈中性:
| ||
D、①和④混合后溶液呈酸性:
|
下列说法正确的是( )
| A、冰和干冰既是纯净物又是化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| D、盐酸和食醋既是化合物又是酸 |
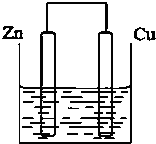 将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.
将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.