题目内容
1.Fe2(SO4)3晶体中铁离子的核外电子排布式为1s2 2s22p6 3s23p63d5.分析 Fe的原子核外电子数为26,失去3个电子生成铁离子,据此分析.
解答 解:Fe的原子核外电子数为26,原子核外电子排布式为1s2 2s22p6 3s23p63d6 4s2,失去3个电子生成铁离子,则铁离子的核外电子排布式为1s2 2s22p6 3s23p63d5,
故答案为:1s2 2s22p6 3s23p63d5.
点评 本题考查了元素原子和离子的电子排布式,题目难度不大,注意注意基础知识的积累,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
1.某兴趣小组的同学发现,将CuSO4溶液与K2CO3溶液混合会产生蓝绿色沉淀.他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究.
(1)【提出假设】假设1:所得沉淀为Cu(OH)2;
假设2:所得沉淀为CuCO3;(填化学式)
假设3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2•nCuCO3].
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水).
【定性探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如装置如图(夹持仪器未画)进行定性实验;
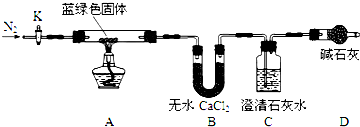
(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设1成立.
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是B(填代号).
A.浓硫酸 B.无水CuSO4 C.碱石灰 D.P2O5
(4)乙同学验证假设3成立的实验现象是A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生.
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是AC(填代号).
A.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
B.Ba(OH)2为强碱,Ca(OH)2为弱碱
C.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
D.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g.则该蓝绿色固体的化学式为2CuCO3•3Cu(OH)2、或3Cu(OH)2•2CuCO3或Cu5(OH)6(CO3)2;A中发生反应的化学方程式为2CuCO3•3Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+3H2O↑+2CO2↑.
(1)【提出假设】假设1:所得沉淀为Cu(OH)2;
假设2:所得沉淀为CuCO3;(填化学式)
假设3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2•nCuCO3].
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水).
【定性探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如装置如图(夹持仪器未画)进行定性实验;

(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设1成立.
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是B(填代号).
A.浓硫酸 B.无水CuSO4 C.碱石灰 D.P2O5
(4)乙同学验证假设3成立的实验现象是A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生.
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是AC(填代号).
| 溶解度(S)/p | 溶度积(Ksp) | 摩尔质量(M)/g•mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
B.Ba(OH)2为强碱,Ca(OH)2为弱碱
C.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
D.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g.则该蓝绿色固体的化学式为2CuCO3•3Cu(OH)2、或3Cu(OH)2•2CuCO3或Cu5(OH)6(CO3)2;A中发生反应的化学方程式为2CuCO3•3Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+3H2O↑+2CO2↑.
2.下列说法不正确的是( )
| A. | 乙醇分子中有1个氢原子与其他氢原子不一样 | |
| B. | 乙醇分子可认为是由乙烷分子中的一个-H被一个-OH取代产生的 | |
| C. | 乙醇分子中的每个碳原子都形成了四个共价键,但显示化合价不是+4价 | |
| D. | 乙醇的相对分子质量为46,相对分子质量为46的有机物就是乙醇 |
9.某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂,下列操作中可能使所测氢氧化钠溶液浓度偏大的是( )
| A. | 酸式滴定管未用标准盐酸润洗,直接装入标准盐酸 | |
| B. | 酸式滴定管滴定前有气泡,滴定后气泡消失 | |
| C. | 滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥 | |
| D. | 读取醋酸体积时,开始仰视读数,滴定结束后俯视读数 |
16.下列各化合物的命名正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | 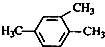 1,3,4-三甲苯 1,3,4-三甲苯 | ||
| C. | CH3CH2CH(OH)CH3 2-丁醇 | D. | 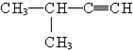 2-甲基-3-丁炔 2-甲基-3-丁炔 |
10.短周期主族元素X、Y、Z、W、Q的原子序数依次增大.X的气态氢化物极易溶于Y的氢化物中.常温下,Z的块状单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液.下列说法正确的是( )
| A. | 元素Y的最高正化合价+6 | |
| B. | 简单离子半径的大小顺序为W>Q>Z>X>Y | |
| C. | 气态氢化物的稳定性:Q>W | |
| D. | 元素W的最高价氧化物对应的水化物酸性比Q的强 |