题目内容
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
A
【解析】
试题分析:某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子,A.CH3COOH是弱酸,部分电离,在溶液中存在电离平衡:CH3COOH CH3COO-+H+。pH=3,则c(H+)=10-3mol/L.c(CH3COOH)> c(H+)=10-3mol/L;NaOH是强碱,完全电离。pH=11,则c(OH-)=10-3mol/L.若二者等体积混合,则酸已经电离的部分恰好被中和,由于破坏了酸的电离平衡,未电离的酸分子将继续电离,使溶液显酸性。正确。B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成。则二者恰好发生中和反应产生CH3COONa。由于该盐是强碱弱酸盐,弱酸根离子CH3COO-会发生水解反应CH3COO-+H2O
CH3COO-+H+。pH=3,则c(H+)=10-3mol/L.c(CH3COOH)> c(H+)=10-3mol/L;NaOH是强碱,完全电离。pH=11,则c(OH-)=10-3mol/L.若二者等体积混合,则酸已经电离的部分恰好被中和,由于破坏了酸的电离平衡,未电离的酸分子将继续电离,使溶液显酸性。正确。B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成。则二者恰好发生中和反应产生CH3COONa。由于该盐是强碱弱酸盐,弱酸根离子CH3COO-会发生水解反应CH3COO-+H2O CH3COOH+ OH-。当最终达到平衡时c(OH-)> c(H+)。溶液显碱性,与题意不符。错误。C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(H+) >c(OH-)或c(Na+)>c(CH3COO-)>c(OH-)>c(H+),否则违背电荷守恒。错误。D.加入适量氨水,若溶液呈中性c(CH3COO-)等于c(Na+)、c(NH4+)之和,若呈酸性,c(CH3COO-)大于c(Na+)、c(NH4+)之和;若呈碱性,则c(CH3COO-)小于c(Na+)、c(NH4+)之和。错误。
CH3COOH+ OH-。当最终达到平衡时c(OH-)> c(H+)。溶液显碱性,与题意不符。错误。C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(H+) >c(OH-)或c(Na+)>c(CH3COO-)>c(OH-)>c(H+),否则违背电荷守恒。错误。D.加入适量氨水,若溶液呈中性c(CH3COO-)等于c(Na+)、c(NH4+)之和,若呈酸性,c(CH3COO-)大于c(Na+)、c(NH4+)之和;若呈碱性,则c(CH3COO-)小于c(Na+)、c(NH4+)之和。错误。
考点:考查含有相同离子的溶液的配制及离子浓度的大小比较的知识。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案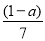 B.
B.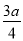 C.
C.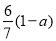 D.
D.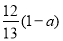
 5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37
5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37
 -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( ) 处,手持试管夹长柄末端,进行加热
处,手持试管夹长柄末端,进行加热