题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、4.6 g组成为C2H6O的有机物,所含C-H键数目一定为0.6NA | ||||
| B、8.7 g MnO2与40 mL 10 mol?L-1的浓盐酸充分反应,生成的氯气分子数为0.1NA | ||||
| C、1 mol Na2O中含有的阴、阳离子总数是3NA而1 mol Na2O2中含有的阴、阳离子总数是4NA | ||||
D、在反应5NH4NO3
|
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、C2H6O可能是乙醇,也可能是甲醚;
B、随着反应的进行,盐酸浓度逐渐降低,当成为稀盐酸时,该反应停止;
C、Na2O2是由钠离子和过氧根离子构成;
D、5个铵根离子中-3价N变为0价,失去15个电子.
B、随着反应的进行,盐酸浓度逐渐降低,当成为稀盐酸时,该反应停止;
C、Na2O2是由钠离子和过氧根离子构成;
D、5个铵根离子中-3价N变为0价,失去15个电子.
解答:
解:A、4.6 g组成为C2H6O的有机物的物质的量为0.1mol,若为乙醇含有C-H键数目为0.5NA,若为甲醚所含C-H键数目为0.6NA,故A错误;
B、随着反应的进行,盐酸浓度逐渐降低,当成为稀盐酸时,该反应停止,因此生成氯气的分子数一定小于0.1NA,故B错误;
C、Na2O2是由钠离子和过氧根离子构成,1 mol Na2O和1 mol Na2O2中含有的阴、阳离子总数都是3NA,故C错误;
D、5个铵根离子中-3价N变为0价,失去15个电子,此时生成了4个氮气分子,当生成4 mol N2,转移电子数为15NA,故D正确;
故选D.
B、随着反应的进行,盐酸浓度逐渐降低,当成为稀盐酸时,该反应停止,因此生成氯气的分子数一定小于0.1NA,故B错误;
C、Na2O2是由钠离子和过氧根离子构成,1 mol Na2O和1 mol Na2O2中含有的阴、阳离子总数都是3NA,故C错误;
D、5个铵根离子中-3价N变为0价,失去15个电子,此时生成了4个氮气分子,当生成4 mol N2,转移电子数为15NA,故D正确;
故选D.
点评:本题考查了有机物的同分异构现象、实验室制取氯气的原理、过氧化钠的组成、转移电子数的计算等知识,难度一般,注意化学反应原理的掌握和灵活应用.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
下列物质能发生催化氧化且产物是2甲基丁醛的是( )
A、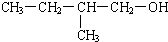 |
B、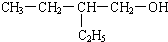 |
C、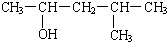 |
D、 |
有机化合物与人类生活水平的提高和人类社会的发展密不可分.下列对有机化合物的认识正确的是( )
| A、碳原子的成键方式多是有机物种类繁多原因之一 |
| B、有机化合物都含有碳、氢元素 |
| C、有机化合物都具有同分异构现象 |
| D、有机化合物都具有可燃性 |
下列反应不属于置换反应的是( )
| A、CuO+H2=Cu+H2O |
| B、C+2CuO=2Cu+CO2↑ |
| C、Fe2O3+3CO=2Fe+3CO2 |
| D、Fe+CuCl2=Cu+FeCl2 |
下列叙述正确的是( )
| A、所有原子中都有质子、中子、电子三种微粒 | ||||||
B、由
| ||||||
C、
| ||||||
D、
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、加入铝粉产生H2 的溶液中:Fe2+、Na+、SO2-4、ClO- |
| B、由水电离的c(H+)=1×10-14mol?L-1的溶液中:Ca2+、K+、Cl-、HCO-3 |
| C、c(H+)/c(OH-)=1012的溶液中:NH+4、Al3+、NO-3、Cl- |
| D、使甲基橙呈红色的溶液:K+、Cl-、SO2-4、S2O2-3 |
对于某酸的酸式盐NaHY的水溶液的下列叙述中,正确的是( )
| A、该酸式盐的水溶液一定显酸性 |
| B、该酸式盐的水溶液一定呈碱性 |
| C、若HY-能水解,水解方程式为HY-+H2O?Y2-+H3O+ |
| D、若HY-能水解,水解方程式为HY-+H2O?H2Y+OH- |
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ |
| B、已知C(石墨,s)═C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2则△H1>△H2 |
| D、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol |
设阿伏加德罗常数的值为NA,下列有关说法正确的是( )
| A、0.5mol苯分子中含有C=C双键数为1.5NA |
| B、2.8g乙烯、丙烯和聚乙烯的混合物中所含碳原子数为0.2NA |
| C、标准状况下,2.24L C5H12含有的共用电子对为1.6NA |
| D、1mol甲基(-CH3)所含的电子总数为8NA |