题目内容
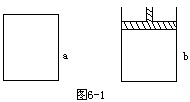
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器压强恒定。在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应: 2NO2 N2O4
△H<0,则以下说法正确的是:(
)
N2O4
△H<0,则以下说法正确的是:(
)
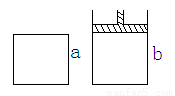
A.反应起始时两容器的反应速率va和vb的关系:va<vb
B.反应过程中两容器内的反应速率va和vb的关系:va<vb
C.反应达到平衡时,两容器内压强相同
D.反应达到平衡时,两容器的NO2的转化率相同
【答案】
B
【解析】起始时温度、浓度和压强都是相同的,所以反应速率相同,A不正确。反应是体积减小的可逆反应,因此在反应过程中b中的压强始终大于a中的压强,因此反应速率快,B正确,C不正确。由于压强大有利于平衡向正反应方向移动,所以b中的转化率大于a中的转化率,D不正确。因此答案选B。

练习册系列答案
相关题目
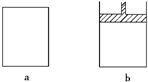 有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应:2NO2?N2O4(正反应放热),则以下说法正确的是( )?
| A、反应起始时反应速率的关系:va<vb? | B、反应过程中反应速率的关系:va<vb? | C、两容器内反应达到平衡所需时间一定相同? | D、反应达到平衡,两容器中的NO2的转化率相同? |
 N2O4
△H<0,则以下说法正确的是
N2O4
△H<0,则以下说法正确的是
 N2O4+Q(Q>0),请用“> ”、“<”或“=”填空:
N2O4+Q(Q>0),请用“> ”、“<”或“=”填空: