题目内容
18.用下列方法制取氢气,反应速率最大的是( )| A. | 冬天,块状锌与2 mol•L-1硫酸溶液反应 | |
| B. | 冬天,粉末状锌与2 mol•L-1硫酸溶液反应 | |
| C. | 夏天,块状锌与2 mol•L-1硫酸溶液反应 | |
| D. | 夏天,粉末状锌与2mol•L-1硫酸溶液反应 |
分析 题中涉及影响反应速率的因素有温度、浓度和固体的表面积大小,一般来说,温度越高、浓度越大,固体的表面积越大,则反应速率越大,反之越小,以此解答.
解答 解:冬天温度低,夏天温度高,所以夏天的反应速率比冬天的高,故A、B错误,在硫酸浓度大小一样的情况下,粉末状的金属锌的反应速率比块状锌的反应速率要快,故C错误,D正确.
故选D.
点评 本题考查化学反应速率的影响因素,侧重于学生的分析能力的考查,为高考高频考点,注意把握影响反应速率的因素,注重相关知识的学习与积累,难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
8.将下列物质按酸、碱、盐、电解质分类排列,正确的是( )
| A. | 硝酸、纯碱、胆矾、铜 | B. | 硫酸、烧碱、小苏打、纯碱 | ||
| C. | 盐酸、乙醇、氯化钠、碘酒 | D. | 醋酸、漂白粉、石灰石、二氧化碳 |
6.以下实验能获得成功的是( )
| A. | 苯和硝基苯直接采用分液的方法分离 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 在溴乙烷中加入NaOH水溶液共热,然后加入稀硝酸至呈酸性,再滴入AgNO3溶液,通过观察有无浅黄色沉淀来检验溴乙烷中的溴元素 | |
| D. | 在蔗糖溶液中加入稀硫酸共热,然后加入银氨溶液水浴加热,通过观察有无银镜生成来检验蔗糖的水解产物中有无还原性糖 |
13.下列说法不正确的是( )
| A. | 1mol葡萄糖在酒化酶作用下水解生成2mol乙醇和2mol二氧化碳 | |
| B. | 在一定条件下CO和氢气作用得到液体燃料的过程是煤的液化途径之一 | |
| C. | 石油的重整可以提高汽油的质量和芳烃的产量 | |
| D. | 往蛋白质溶液中加入饱和硫酸钠溶液,产生的沉淀再加水又可溶解 |
3.一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示:下列判断正确的是( )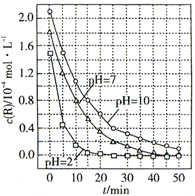

| A. | 溶液酸性越强,R的降解速率越小 | |
| B. | R的起始浓度越小,降解速率越大 | |
| C. | 在0~50 min之间,pH=2和pH=7时R的降解百分率相等 | |
| D. | 在20~25 min之间,pH=10时R的平均降解速率为0.02 mol•L-1•min-1 |
10.下列物质的分子中,既有“s_pσ键,又有p_pσ键的是( )
| A. | H2O | B. | OF2 | C. | HClO | D. | N2 |

 化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活.
化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活.