��Ŀ����
 �ϳɰ������ķ���ʹ��ҵ���˹��̵���Ϊ��ʵ��
�ϳɰ������ķ���ʹ��ҵ���˹��̵���Ϊ��ʵ����1����֪N2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1����һ�������·�Ӧʱ�������ɱ�״����33.6L NH3ʱ���ų�������Ϊ
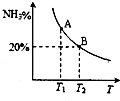
��2���ϳɰ������ϵ��ƽ��״̬ʱNH3�İٷֺ������¶ȵĹ�ϵ��ͼ��ʾ����ͼ��֪��
���¶�T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1
��T2�¶�ʱ����1L���ܱ������м���2.1mol N2��1.5mol H2����10min�ﵽƽ�⣬��v��H2��=
��3����ҵ����CO2��NH3��Ӧ�������أ�CO2��g��+2NH3��g��?H2O��l��+CO��NH2��2��l����H��
��һ��ѹǿ�²���������ݣ�
| �¶�/�� CO2ת����%
|
100 | 150 | 200 | ||
| 1 | 19.6 | 27.1 | 36.6 | ||
| 1.5 | a | b | c | ||
| 2 | d | e | f |
�ڴ����غϳ����ڳ������������Ժ���һ������CO2��NH3��Ӧ��δ���
���㣺��ѧƽ��ļ���,�йط�Ӧ�ȵļ���,��ѧƽ�⽨���Ĺ���,��ѧƽ���Ӱ������
ר�⣺�����������������
��������1�������Ȼ�ѧ����ʽ������ϵ�������������n=
���������ʵ�������Ȼ�ѧ����ʽ����õ���
��2����ͼ�������A�㰱����������B�㣬˵���¶�Խ�ߣ���������Խ�٣�ƽ��������У�ƽ�ⳣ����С�����º�ѹ����������壬�������ѹǿ��С��ƽ���������������ķ������У�������У�
������ƽ��ת���ʼ������ɵİ��������ƽ������ʽ��ʽ���㣬��Ӧ����V=
������ƽ�ⳣ�������ƽ��Ũ�ȼ���õ����������Ũ�ȼ���Ũ���̺�ƽ�ⳣ���Ƚϣ�
��3���ٷ���ͼ���������Ͷ�����̼���ʵ���֮�ȵ���1�����¶����ߣ�CO2ת��������˵����Ӧ������У����������ȷ�Ӧ�������Ͷ�����̼���ʵ���֮������ƽ��������У�������̼ת�����������ݻ�ѧƽ��Ӱ�����غ�ƽ������ʽ�����жϣ�
��ѭ������ԭ�ϣ�
| V |
| 22.4 |
��2����ͼ�������A�㰱����������B�㣬˵���¶�Խ�ߣ���������Խ�٣�ƽ��������У�ƽ�ⳣ����С�����º�ѹ����������壬�������ѹǿ��С��ƽ���������������ķ������У�������У�
������ƽ��ת���ʼ������ɵİ��������ƽ������ʽ��ʽ���㣬��Ӧ����V=
| ��c |
| ��t |
��3���ٷ���ͼ���������Ͷ�����̼���ʵ���֮�ȵ���1�����¶����ߣ�CO2ת��������˵����Ӧ������У����������ȷ�Ӧ�������Ͷ�����̼���ʵ���֮������ƽ��������У�������̼ת�����������ݻ�ѧƽ��Ӱ�����غ�ƽ������ʽ�����жϣ�
��ѭ������ԭ�ϣ�
���
�⣺��1����֪N2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1����һ�������·�Ӧʱ�������ɱ�״����33.6L NH3ʱ���ʵ���=
=1.5mol���ų�������=
=69.15kJ��
�ʴ�Ϊ��69.15kJ��
��2����ͼ�������A�㰱����������B�㣬˵���¶�Խ�ߣ���������Խ�٣�ƽ��������У�ƽ�ⳣ����С���¶�T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2�����º�ѹ����������壬�������ѹǿ��С��ƽ���������������ķ������У�������У�ƽ�������ƶ���
�ʴ�Ϊ����������
��T2�¶�ʱ��ͼ�������֪��ƽ��ʱ��������Ϊ20%����1L���ܱ������м���2.1mol N2��1.5mol H2����10min�ﵽƽ�⣬�����ĵ���Ũ��Ϊx��
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 2.1 1.5 0
�仯����mol/L�� x 3x 2x
ƽ������mol/L�� 2.1-x 1.5-3x 2x
ƽ��ʱ��������Ϊ20%��
=20%
x=0.3mol/L
��v��H2��=
=0.09 mol?L-1?min-1��
ƽ��Ũ��c��NH3��=0.6mol/L��c��H2��=0.6mol/L��c��N2��=1.8mol/L
K=
=0.93
�ﵽƽ�����������������ͨ��N2��H2��NH3��0.4mol��������Ũ��Ϊ����NH3��=0.6mol/L+0.4mol/L=1mol/L��c��H2��=0.6mol/L+0.4mol/L=1mol/L��c��N2��=1.8mol/L+0.4mol/L=2.2mol/L
Q=
=0.45��K=0.93����Ӧ������У�
�ʴ�Ϊ��0.09 mol?L-1?min-1�����ң�
��3���ٷ���ͼ���������Ͷ�����̼���ʵ���֮�ȵ���1�����¶����ߣ�CO2ת��������˵����Ӧ������У����������ȷ�Ӧ����H��0�������Ͷ�����̼���ʵ���֮������ƽ��������У�������̼ת��������a��d������ͼ�����ݷ�Ӧ�����ȷ�Ӧ��b��c��e��f��b��e���õ���b��f��
�ʴ�Ϊ��������������
�ڴ����غϳ����ڳ������������Ժ���һ������CO2��NH3��Ӧ���������³���ϳ����ڣ�ѭ�����ã����ԭ�������ʣ�
�ʴ�Ϊ�����������³���ϳ����ڣ�ѭ�����ã����ԭ�������ʣ�
| 33.6L |
| 22.4L/mol |
| 1.5mol��92.2KJ |
| 2mol |
�ʴ�Ϊ��69.15kJ��
��2����ͼ�������A�㰱����������B�㣬˵���¶�Խ�ߣ���������Խ�٣�ƽ��������У�ƽ�ⳣ����С���¶�T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2�����º�ѹ����������壬�������ѹǿ��С��ƽ���������������ķ������У�������У�ƽ�������ƶ���
�ʴ�Ϊ����������
��T2�¶�ʱ��ͼ�������֪��ƽ��ʱ��������Ϊ20%����1L���ܱ������м���2.1mol N2��1.5mol H2����10min�ﵽƽ�⣬�����ĵ���Ũ��Ϊx��
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 2.1 1.5 0
�仯����mol/L�� x 3x 2x
ƽ������mol/L�� 2.1-x 1.5-3x 2x
ƽ��ʱ��������Ϊ20%��
| 2x |
| 3.6--2x |
x=0.3mol/L
��v��H2��=
| 3��0.3mol/L |
| 10min |
ƽ��Ũ��c��NH3��=0.6mol/L��c��H2��=0.6mol/L��c��N2��=1.8mol/L
K=
| 0��62 |
| 0��63��1.8 |
�ﵽƽ�����������������ͨ��N2��H2��NH3��0.4mol��������Ũ��Ϊ����NH3��=0.6mol/L+0.4mol/L=1mol/L��c��H2��=0.6mol/L+0.4mol/L=1mol/L��c��N2��=1.8mol/L+0.4mol/L=2.2mol/L
Q=
| 12 |
| 13��2.2 |
�ʴ�Ϊ��0.09 mol?L-1?min-1�����ң�
��3���ٷ���ͼ���������Ͷ�����̼���ʵ���֮�ȵ���1�����¶����ߣ�CO2ת��������˵����Ӧ������У����������ȷ�Ӧ����H��0�������Ͷ�����̼���ʵ���֮������ƽ��������У�������̼ת��������a��d������ͼ�����ݷ�Ӧ�����ȷ�Ӧ��b��c��e��f��b��e���õ���b��f��
�ʴ�Ϊ��������������
�ڴ����غϳ����ڳ������������Ժ���һ������CO2��NH3��Ӧ���������³���ϳ����ڣ�ѭ�����ã����ԭ�������ʣ�
�ʴ�Ϊ�����������³���ϳ����ڣ�ѭ�����ã����ԭ�������ʣ�
���������⿼�����Ȼ�ѧ����ʽ���㣬ͼ������жϻ�ѧƽ�⡢��Ӧ���ʡ�ƽ�ⳣ������Ӧ�ã�����ƽ���ƶ�ԭ���ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
�����Ŀ
����ͬ��������ȫȼ�ռ��顢���顢��ϩ����ʹ������ˮ��������ͬ״�����������ȣ�����������������������ǣ�������
| A��8��?11��?14 |
| B��4��?22��?7 |
| C��1��?2��?1 |
| D��2��?1��?2 |
��ȥ���������е��������ʣ����з������е��ǣ�������
| A�����Ҵ���Ũ���ᣬ���� |
| B����NaOH��Һ�������Һ |
| C��ֱ�ӷ�Һ |
| D���ӱ���Na2CO3��Һ�������Һ |
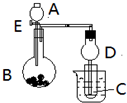 ����ͼ��ʾװ�ý���ʵ�飬��A��μ���B�У�
����ͼ��ʾװ�ý���ʵ�飬��A��μ���B�У�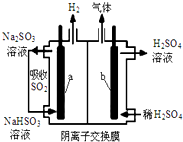 ��ⷨ����Ⱦ�������й㷺Ӧ�ã���������������Ӧ�ã�
��ⷨ����Ⱦ�������й㷺Ӧ�ã���������������Ӧ�ã�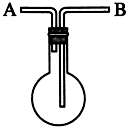 ������ͼװ���ռ�����7�����壺����������Ż�A��B��
������ͼװ���ռ�����7�����壺����������Ż�A��B��