题目内容
实验室中用锌和稀硫酸反应制取氢气.
(1)要制取3.36L(标准状况)气体,需要1mol/L H2SO4多少毫升?
(2)某同学用向下排空气法收集氢气,测得所收集气体密度是纯氢气密度的1.2倍.求该气体中氢气所占的体积分数(设空气的平均相对分子质量为29).
(1)要制取3.36L(标准状况)气体,需要1mol/L H2SO4多少毫升?
(2)某同学用向下排空气法收集氢气,测得所收集气体密度是纯氢气密度的1.2倍.求该气体中氢气所占的体积分数(设空气的平均相对分子质量为29).
考点:化学方程式的有关计算,阿伏加德罗定律及推论
专题:计算题
分析:(1)先计算出标况下3.36L氢气的物质的量,再根据氢原子守恒计算出需要1mol/L的稀硫酸的体积;
(2)根据相对密度计算出混合气体的平均摩尔质量,再设出混合气体中氢气、空气的物质的量,根据氢气、空气的平均摩尔质量列式计算出氢气位置物质的量之比及体积分数.
(2)根据相对密度计算出混合气体的平均摩尔质量,再设出混合气体中氢气、空气的物质的量,根据氢气、空气的平均摩尔质量列式计算出氢气位置物质的量之比及体积分数.
解答:
解:(1)标准状况下,3.36L氢气的物质的量为:n(H2)=
=0.15mol,根据反应方程式Zn+H2SO4=ZnSO4+H2↑可知,反应消耗的硫酸的物质的量为:n(H2SO4)=n(H2)=0.15mol,
需要1mol/L H2SO4的体积为:V=
=0.15L=150mL,
答:需要1mol/L的硫酸的体积为150mL;
(2)所收集气体密度是纯氢气密度的1.2倍,根据M=ρVm可知:相同条件下气体的摩尔质量与密度成正比,
则:混合气体的平均摩尔质量为:M=2g/mol×1.2=2.4g/mol,
设混合气体中含有xmol氢气、ymol空气,则:
=2.4g/mol,
解得x:y=133:2,
混合气体中氢气的体积分数为:
×100%≈98.5%,
答:该气体中氢气所占的体积分数为98.5%.
| 3.36L |
| 22.4L/mol |
需要1mol/L H2SO4的体积为:V=
| 0.15mol |
| 1mol/L |
答:需要1mol/L的硫酸的体积为150mL;
(2)所收集气体密度是纯氢气密度的1.2倍,根据M=ρVm可知:相同条件下气体的摩尔质量与密度成正比,
则:混合气体的平均摩尔质量为:M=2g/mol×1.2=2.4g/mol,
设混合气体中含有xmol氢气、ymol空气,则:
| 2g/mol×xmol+29g/mol×ymol |
| xmol+ymol |
解得x:y=133:2,
混合气体中氢气的体积分数为:
| 133 |
| 133+2 |
答:该气体中氢气所占的体积分数为98.5%.
点评:本题考查了有关化学方程式的计算,题目难度中等,注意掌握物质的量与气体摩尔体积、摩尔质量等物理量之间关系,明确利用化学方程式进行计算的方法.

练习册系列答案
相关题目
下列说法正确的是( )
| A、28 g乙烯和丁烯的混合气体中含有的碳原子的物质的量为2 mol |
| B、22.4 L氯气与足量铁粉充分反应,转移的电子的物质的量为2mol |
| C、某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、常温下,1 mol Fe与足量的浓HNO3反应,转移3NA个电子 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A、标准状况下,1L庚烷所含有的分子数为
| ||
| B、1mol甲基(-CH3)所含电子数为9NA | ||
| C、标准状况下,C2H6和C2H4的混合气体22.4L,所含的电子数约为16NA | ||
| D、26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
下列离子反应方程式正确的是( )
| A、氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| B、钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| C、Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、FeCl3溶液刻蚀铜制的印刷电路板:Cu+Fe3+=Cu2++Fe2+ |
对于反应:A(g)+qB(g)=pC(g),经t秒后C的浓度增加了m mol/L,则用B浓度的变化表示的反应速率大小为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
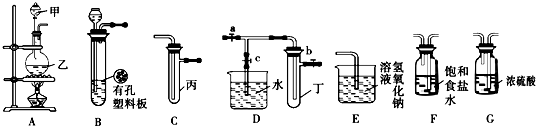
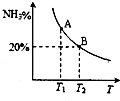 合成氨技术的发明使工业化人工固氮成为现实.
合成氨技术的发明使工业化人工固氮成为现实.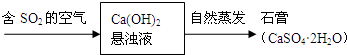

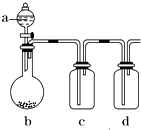 有几个实验小组的同学,利用右图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.
有几个实验小组的同学,利用右图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.