جâؤ؟ؤعبف
،¾جâؤ؟،؟ج¼،¢µھ،¢ءٍ¼°ئن»¯؛دخï¶شةْ²ْ،¢ةْ»îسذضطزھµؤزâزه،£
(1)زش![]() سë
سë![]() خھشءد؟ة؛د³ةؤٍثط،£زرضھ£؛
خھشءد؟ة؛د³ةؤٍثط،£زرضھ£؛
¢ظ![]()
![]()
¢ع![]()
![]()
¢غ![]()
![]()
ذ´³ِNH3؛حCO2؛د³ةؤٍثط؛حز؛ج¬ث®µؤبب»¯ر§·½³جت½________،£
(2)¸كخآدآ£¬CO2سë×مء؟µؤج¼شعأـ±صبفئ÷ضذتµدض·´س¦£؛![]() ،£دٍبف»خھ1Lµؤ؛مبفبفئ÷ضذ¼سبë0.2molCO2£¬شع²»ح¬خآ¶بدآ´ïµ½ئ½؛âت±CO2µؤخïضتµؤء؟إ¨¶بثوخآ¶بµؤ±ن»¯بçح¼ثùت¾،£شٍ¸أ·´س¦خھ________(جî،°·إبب،±»ٍ،°خüبب،±)·´س¦£»ؤ³خآ¶بدآبôدٍ¸أئ½؛âجهدµضذشظح¨بë0.2molCO2£¬´ïµ½ذآئ½؛â؛َ£¬جهدµضذCOµؤ°ظ·ض؛¬ء؟________(جî،°±ن´َ،±،¢،°±نذ،،±»ٍ،°²»±ن،±)،£
،£دٍبف»خھ1Lµؤ؛مبفبفئ÷ضذ¼سبë0.2molCO2£¬شع²»ح¬خآ¶بدآ´ïµ½ئ½؛âت±CO2µؤخïضتµؤء؟إ¨¶بثوخآ¶بµؤ±ن»¯بçح¼ثùت¾،£شٍ¸أ·´س¦خھ________(جî،°·إبب،±»ٍ،°خüبب،±)·´س¦£»ؤ³خآ¶بدآبôدٍ¸أئ½؛âجهدµضذشظح¨بë0.2molCO2£¬´ïµ½ذآئ½؛â؛َ£¬جهدµضذCOµؤ°ظ·ض؛¬ء؟________(جî،°±ن´َ،±،¢،°±نذ،،±»ٍ،°²»±ن،±)،£

(3)ز»¶¨ء؟µؤ![]() سë×مء؟µؤج¼شعجه»؟ة±نµؤ؛مر¹أـ±صبفئ÷ضذ·´س¦£؛
سë×مء؟µؤج¼شعجه»؟ة±نµؤ؛مر¹أـ±صبفئ÷ضذ·´س¦£؛![]() £¬ئ½؛âت±جهدµضذئّجهجه»·ضتسëخآ¶بµؤ¹طدµبçح¼ثùت¾£؛
£¬ئ½؛âت±جهدµضذئّجهجه»·ضتسëخآ¶بµؤ¹طدµبçح¼ثùت¾£؛

¢ظ650،وت±£¬·´س¦´ïئ½؛â؛َ![]() µؤ×ھ»¯آتخھ________،£
µؤ×ھ»¯آتخھ________،£
¢ع![]() ،وت±£¬ئ½؛â³£ت
،وت±£¬ئ½؛â³£ت![]() ________
________![]() (سأئ½؛â·ضر¹´ْجوئ½؛âإ¨¶ب¼ئثم£¬·ضر¹
(سأئ½؛â·ضر¹´ْجوئ½؛âإ¨¶ب¼ئثم£¬·ضر¹![]() ×ـر¹
×ـر¹![]() جه»·ضت)،£
جه»·ضت)،£
(4)![]() سë
سë![]() ؤـ·¢ةْ·´س¦£؛
ؤـ·¢ةْ·´س¦£؛![]()
![]() شع¹ج¶¨جه»µؤأـ±صبفئ÷ضذ£¬ت¹سأؤ³ضض´ك»¯¼ء£¬¸ؤ±نشءدئّإن±ب½ّذذ¶à´ختµرé(¸÷´ختµرéµؤخآ¶ب؟ةؤـدàح¬£¬ز²؟ةؤـ²»ح¬)£¬²â¶¨
شع¹ج¶¨جه»µؤأـ±صبفئ÷ضذ£¬ت¹سأؤ³ضض´ك»¯¼ء£¬¸ؤ±نشءدئّإن±ب½ّذذ¶à´ختµرé(¸÷´ختµرéµؤخآ¶ب؟ةؤـدàح¬£¬ز²؟ةؤـ²»ح¬)£¬²â¶¨![]() µؤئ½؛â×ھ»¯آت،£²؟·ضتµرé½ل¹ûبçح¼ثùت¾£؛
µؤئ½؛â×ھ»¯آت،£²؟·ضتµرé½ل¹ûبçح¼ثùت¾£؛

¢ظµ±بفئ÷ؤع________(جî±ê؛إ)²»شظثوت±¼نµؤ±ن»¯¶ّ¸ؤ±نت±£¬·´س¦´ïµ½ئ½؛â×´ج¬،£
A£®ئّجهµؤر¹ا؟ B£®ئّجهµؤئ½¾ùؤ¦¶ûضتء؟ C£®ئّجهµؤأـ¶ب D£®![]() µؤجه»·ضت
µؤجه»·ضت
¢عبç¹ûزھ½«ح¼ضذCµمµؤئ½؛â×´ج¬¸ؤ±نخھBµمµؤئ½؛â×´ج¬£¬س¦²ةب،µؤ´ëت©تا________،£
¢غبôAµم¶شس¦تµرéضذ£¬![]() µؤئًت¼إ¨¶بخھ
µؤئًت¼إ¨¶بخھ![]() £¬¾¹
£¬¾¹![]() ´ïµ½ئ½؛â×´ج¬£¬¸أت±¶خ»¯ر§·´س¦ثظآت
´ïµ½ئ½؛â×´ج¬£¬¸أت±¶خ»¯ر§·´س¦ثظآت![]() ________
________![]() ،£
،£
¢ـح¼ضذC،¢Dء½µم¶شس¦µؤخآ¶ب·ض±ًخھ![]() ،و؛ح
،و؛ح![]() ،و£¬ح¨¹¼ئثمإذ¶د
،و£¬ح¨¹¼ئثمإذ¶د![]() ________
________![]() (جî،°
(جî،°![]() ،±،¢،°
،±،¢،°![]() ،±»ٍ،°
،±»ٍ،°![]() ،±)،£
،±)،£
،¾´ً°¸،؟![]()
![]() خüبب ±نذ، 25% 0.5 D ½µµحخآ¶ب
خüبب ±نذ، 25% 0.5 D ½µµحخآ¶ب ![]()
![]()
،¾½âخِ،؟
±¾جâ×غ؛د؟¼²ى¸اث¹¶¨آة؛ح»¯ر§ئ½؛â³£تµؤ¼ئثم£¬»¯ر§ئ½؛â³£تµؤ¼ئثم³£سأب¶خت½ہ´½ّذذ¼ئثم£¬¶شسع·´س¦![]() £¬سأئ½؛â·ضر¹´ْجوئ½؛âإ¨¶ب¼ئثمµؤ»¯ر§ئ½؛â³£تµؤ±ي´ïت½خھ£؛
£¬سأئ½؛â·ضر¹´ْجوئ½؛âإ¨¶ب¼ئثمµؤ»¯ر§ئ½؛â³£تµؤ±ي´ïت½خھ£؛![]() ،£
،£
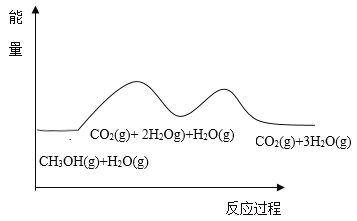
(1)¸ù¾ف¸اث¹¶¨آة¼ئثم£¨1£©+£¨2£©-£¨3£©µأ![]() سë
سë![]() ؛د³ةؤٍثطµؤبب»¯ر§·½³جت½خھ£؛
؛د³ةؤٍثطµؤبب»¯ر§·½³جت½خھ£؛![]() £»
£»![]() £¬¹ت±¾جâ´ً°¸خھ£؛
£¬¹ت±¾جâ´ً°¸خھ£؛![]() £»
£»![]() ،£
،£
(2)ثو×إخآ¶بµؤة¸ك£¬CO2µؤخïضتµؤء؟إ¨¶بضً½¥¼ُذ،£¬ثµأ÷ئ½؛âصدٍزئ¶¯£¬زٍ´ث¸أ·´س¦تôسعخüبب·´س¦£»؛مبفبفئ÷ضذ³نبë¶رُ»¯ج¼؟ةزش؟´×ِ£¬¶رُ»¯ج¼دبسëج¼شعئنثûبفئ÷·´س¦´ïµ½ئ½؛â؛َ£¬شظ»ى؛د°رجه»ثُذ،ضءشت¼جه»£¬د൱سعشِ´َر¹ا؟£¬شٍئ½؛âدٍؤو·´س¦·½دٍ½ّذذ£¬´ïµ½ذآئ½؛â؛َ£¬جهدµضذCOµؤ°ظ·ض؛¬ء؟¼ُذ،£¬¹ت±¾جâ´ً°¸خھ£؛خüبب£»±نذ،£»
(3)سةح¼؟ةزشضھµہ£¬650،وت±£¬·´س¦´ïµ½ئ½؛â؛َCOµؤجه»·ضتخھ40%£¬ةè؟ھت¼·´س¦ت±¼سبëµؤ¶رُ»¯ج¼خھ1mol£¬×ھ»¯ءثx mol£¬شٍسذ£؛

ثùزش![]() £¬¼ئثم³ِx=0.25mol£¬شٍ¶رُ»¯ج¼µؤ×ھ»¯آتخھ25%£»
£¬¼ئثم³ِx=0.25mol£¬شٍ¶رُ»¯ج¼µؤ×ھ»¯آتخھ25%£»
![]() ،وت±£¬ز»رُ»¯ج¼؛ح¶رُ»¯ج¼µؤجه»·ضت¾ùخھ50%£¬ شٍ
،وت±£¬ز»رُ»¯ج¼؛ح¶رُ»¯ج¼µؤجه»·ضت¾ùخھ50%£¬ شٍ![]() £¬¹ت±¾جâ´ً°¸خھ£؛25%£»0.5£»
£¬¹ت±¾جâ´ً°¸خھ£؛25%£»0.5£»
(4) ¢ظA£¬·´س¦ا°؛َئّجهخïضتµؤء؟²»±ن£¬ئّجهµؤر¹ا؟ت¼ضص²»±ن£¬²»ؤـثµأ÷·´س¦´ïµ½ئ½؛â×´ج¬£¬¹تA´يخَ£»
B،¢ئّجهضتء؟²»±ن£¬ئّجهخïضتµؤء؟²»±ن£¬ئّجهµؤئ½¾ùؤ¦¶ûضتء؟ت¼ضص²»±ن£¬²»ؤـثµأ÷·´س¦´ïµ½ئ½؛â×´ج¬£¬¹تB´يخَ£»
C،¢·´س¦ا°؛َئّجهضتء؟²»±نئّجهجه»²»±ن£¬ئّجهµؤأـ¶بت¼ضص²»±ن£¬²»ؤـثµأ÷·´س¦´ïµ½ئ½؛â×´ج¬£¬¹تC´يخَ£»
D،¢NO2µؤجه»·ضت²»±نتائ½؛â±êض¾£¬¹تDصب·£»زٍ´ث£¬±¾جâصب·´ً°¸تا£؛D£»
¢عبç¹ûزھ½«ح¼ضذCµمµؤئ½؛â×´ج¬¸ؤ±نخھBµمµؤئ½؛â×´ج¬£¬ئ½؛â×ھ»¯آتشِ´َ£¬ئ½؛âصدٍ½ّذذ£¬ص·´س¦خھ·إبب·´س¦£¬½µµحخآ¶بئ½؛âصدٍ½ّذذ£¬زٍ´ث£¬±¾جâصب·´ً°¸تا£؛½µµحخآ¶ب£»
¢غAµمئ½؛â×ھ»¯آتخھ50%£¬n(NO2)£؛n(SO2)=0.4£¬SO2(g)µؤئًت¼إ¨¶بخھcomol /L£¬NO2ئًت¼إ¨¶بc(NO2)=0.4 comol /L£¬·´س¦µؤ¶رُ»¯µھإ¨¶ب=0. 4comol/ L،ء50%=0.2comol/L£¬¸أت±¶خ»¯ر§·´س¦ثظآتV(NO2)=![]() =
=![]() mol/Lmin£¬زٍ´ث£¬±¾جâصب·´ً°¸تا£؛
mol/Lmin£¬زٍ´ث£¬±¾جâصب·´ً°¸تا£؛![]() £»
£»
(4 NO2(g)+SO2(g)![]() SO3(g)+NO(g)£¬،÷H=-41.8kJ/mol£¬·´س¦خھ·إبب·´س¦£¬n(NO2)£؛n(SO2)=1£¬SO2(g)µؤئًت¼إ¨¶بخھcomol/L£¬c(NO2)= comol/L£¬ح¼ضذC،¢Dء½µم¶شس¦µؤتµرéخآ¶ب·ض±ًخھTc؛حTd£¬Cµم¶رُ»¯µھ×ھ»¯آتخھ50%£¬
SO3(g)+NO(g)£¬،÷H=-41.8kJ/mol£¬·´س¦خھ·إبب·´س¦£¬n(NO2)£؛n(SO2)=1£¬SO2(g)µؤئًت¼إ¨¶بخھcomol/L£¬c(NO2)= comol/L£¬ح¼ضذC،¢Dء½µم¶شس¦µؤتµرéخآ¶ب·ض±ًخھTc؛حTd£¬Cµم¶رُ»¯µھ×ھ»¯آتخھ50%£¬

ئ½؛â³£تK=1،£
Dµم¶رُ»¯ج¼µؤ×ھ»¯آتخھ40%£¬n(NO2)£؛n(SO2)=1.5£¬SO2(g)µؤئًت¼إ¨¶بخھcomol/L£¬c(NO2)= 1.5comol/L£¬شٍ

ئ½؛â³£تK=1،£
ئ½؛â³£تدàح¬£¬ثµأ÷·´س¦خآ¶بدàح¬£¬Tc=Td£¬زٍ´ث£¬±¾جâصب·´ً°¸£؛=،£