题目内容
17.当水和铷与另一碱金属的合金7.8g完全反应时,放出的氢气在标准状况下为0.2g,则合金中另一金属可能是( )| A. | 锂 | B. | 钠 | C. | 钾 | D. | 铯 |
分析 钾和另一种碱金属在化合物中的化合价均为+1价,计算出氢气的物质的量,然后根据2M+2H2O═2MOH+H2↑计算金属的物质的量及摩尔质量,利用平均摩尔质量的来解答.
解答 解:氢气的物质的量为:$\frac{0.2g}{2g/mol}$=0.1mol,
由2M+2H2O═2MOH+H2↑,
2 1
0.2mol 0.1mol
则金属的平均摩尔质量为:$\frac{7.8g}{0.2mol}$=39g/mol,
铷的摩尔质量为85.5g/mol,则另一种碱金属的摩尔质量一定小于39g/mol,
所以另一碱金属可能是Li或Na,
故选AB.
点评 本题考查了混合物反应的计算,题目难度中等,注意掌握讨论法、平均摩尔质量法在化学计算中的应用,明确常见物质性质及反应原理为解答关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.N2O3是硝酸的酸酐,在一定条件下可由4NO2(g)+O2(g)?2N2O3(g)△H<0合成.T1℃时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如下表:
下列说法不正确的是( )
| 时间/s | 0 | 5 | 10 | 15 |
| c(NO2)mol/L | 4.00 | 2.52 | 2.00 | c3 |
| c(O2)mol/L | 1.00 | c1 | c2 | 0.50 |
| A. | 5s内O2的反应速率为0.074mol/L•s) | |
| B. | T1℃时平衡常数为0.125,平衡时NO2和O2的转化率均为50% | |
| C. | T1℃时平衡常数为K1,T2℃时平衡常数为K2,若T1>T2,则K1<K2 | |
| D. | 其它条件不变,将容器的体积的压缩到原来的一半,则重新达到平衡时c(N2O3)<2mol/L |
12.在实验室里,下列除去杂质的方法正确的是 ( )
| A. | 溴苯中混有溴,加入KI溶液,用汽油萃取出溴 | |
| B. | 乙烷中混有乙烯,在一定条件下反应通入氢气,使乙烯转化为乙烷 | |
| C. | 硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液 | |
| D. | 乙烷中混有CO2,将其通入碳酸氢钠溶液洗气后干燥 |
2.下列关于有机化合物的说法不正确的是( )
| A. | 用四氯化碳可以萃取乙酸水溶液中的乙酸 | |
| B. | 丁烷有两种同分异构体 | |
| C. | 乙烯可以与氢气发生加成反应,也可发生自身加聚反应生成聚乙烯 | |
| D. | 纤维素、淀粉和蛋白质都是高分子化合物 |
9.25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )
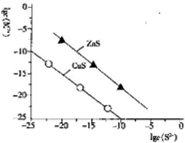

| A. | Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) | |
| B. | 25℃时K甲(CuS)均为1×10-28 | |
| C. | 向l00mLZn2+、Cu2+均为10-5mol•L-1 的混合溶液中逐滴加入10-4mol•L-1 Na2S溶液,Zn2+先沉淀 | |
| D. | 向Cu2+浓度为10-5mol•L-1工业废水中加入ZnS粉末,会有CuS沉淀析出 |
6.下列关于AlCl3的说法中正确的是( )
| A. | AlCl3溶液中还可能大量存在:H+、NH4+、SO42-、NO3- | |
| B. | AlCl3溶液与过量的氨水反应的离子方程式为:Al3++4NH3•H2O═4NH4++AlO2-+2H2O | |
| C. | 若NA为阿伏伽德罗常数的值,则1L0.1mol•L-1的AlCl3溶液中Al3+的数目为0.1NA | |
| D. | 工业上可用电解熔融的AlCl3来制取金属Al |
12.月球土壤中含有较丰富的${\;}_{2}^{3}$He,在地球上氦元素主要以${\;}_{2}^{4}$He的形式存在,下列说法正确的是( )
| A. | ${\;}_{2}^{3}$He代表原子核内有2个质子和3个中子的氦原子 | |
| B. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He分别含有1和2个质子 | |
| C. | ${\;}_{2}^{3}$He 和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{3}$He的最外层电子数为1,所以${\;}_{2}^{3}$He 具有较强的金属性 |


 ;
; ;
; .
.
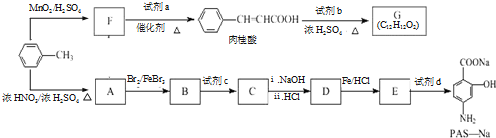
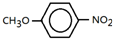
 ;由F生成一硝化产物的化学方程式为:
;由F生成一硝化产物的化学方程式为: +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O,芳香化合物F的名称是对苯二甲酸.
+H2O,芳香化合物F的名称是对苯二甲酸.