题目内容
一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.
(1)在人体中进行Fe2+
Fe3+的转化时,①中的Fe2+作 剂,②中的Fe3+作 剂;
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂;
某学习小组设计实验证明维生素C的性质,要求写出:
实验:取适量FeCl3溶液,加入KSCN溶液,再加入过量维生素C,现象: .
维生素可根据其溶解性的不同分为 性维生素和 性维生素两大类.
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐.此反应的离子方程式为
(4)2007年5月24日中央电视台报道,继“食盐加碘”后,我国又将启动“酱油加铁”工程.“酱油加铁”的意义是 (填序号).
①减少厨房污染物 ②预防缺铁性贫血病 ③补充人体需要的铁元素
(5)通常所指的三大合成材料是
①合成橡胶、合成纤维、复合材料 ②涂料、塑料、黏合剂
③合成橡胶、合成纤维、塑料 ④合成纤维、黏合剂、复合材料
(6)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉.
写出该抗酸药发挥功效时的离子方程式: 、 .
(1)在人体中进行Fe2+
| ② |
| ① |
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作
某学习小组设计实验证明维生素C的性质,要求写出:
实验:取适量FeCl3溶液,加入KSCN溶液,再加入过量维生素C,现象:
维生素可根据其溶解性的不同分为
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐.此反应的离子方程式为
(4)2007年5月24日中央电视台报道,继“食盐加碘”后,我国又将启动“酱油加铁”工程.“酱油加铁”的意义是
①减少厨房污染物 ②预防缺铁性贫血病 ③补充人体需要的铁元素
(5)通常所指的三大合成材料是
①合成橡胶、合成纤维、复合材料 ②涂料、塑料、黏合剂
③合成橡胶、合成纤维、塑料 ④合成纤维、黏合剂、复合材料
(6)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉.
写出该抗酸药发挥功效时的离子方程式:
考点:微量元素对人体健康的重要作用,铁盐和亚铁盐的相互转变,药物的主要成分和疗效,合成材料
专题:化学应用
分析:(1)元素的化合价升高,作还原剂,元素的化合价降低,作氧化剂;
(2)服用维生素C,可使食物中的Fe3+还原成Fe2+,说明维生素C具有还原性,可用KSCN检验,维生素具有水溶性和脂溶性两类;
(3)铁与盐酸反应生成氯化亚铁和氢气;
(4)铁是合成血红蛋白的主要元素,缺乏会患缺铁性贫血;
(5)合成材料主要有三大类:塑料、合成纤维、合成橡胶;
(6)根据化学方程式改写离子方程式.
(2)服用维生素C,可使食物中的Fe3+还原成Fe2+,说明维生素C具有还原性,可用KSCN检验,维生素具有水溶性和脂溶性两类;
(3)铁与盐酸反应生成氯化亚铁和氢气;
(4)铁是合成血红蛋白的主要元素,缺乏会患缺铁性贫血;
(5)合成材料主要有三大类:塑料、合成纤维、合成橡胶;
(6)根据化学方程式改写离子方程式.
解答:
解:(1)Fe2+→Fe3+的转化时,元素的化合价升高,作还原剂;Fe3+→Fe2+转化时,元素的化合价降低,作氧化剂,
故答案为:还原;氧化;
(2))服用维生素C,可使食物中的Fe3+还原成Fe2+,说明维生素C具有还原性,在反应中为还原剂,被氧化,可用FeCl3溶液和KSCN溶液进行检验,在红色溶液中滴加维生素C,如溶液血红色褪去,说明维生素C具有还原性,能将Fe3+还原为Fe2+,维生素可根据其溶解性的不同分为脂溶性维生素和水溶性维生素,维生素C为水溶性维生素,故答案为:还原;先变红后褪色;水溶;脂溶;
(3)铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐的化学反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(4)铁是合成血红蛋白的主要元素,缺乏会患缺铁性贫血,酱油加铁可补充人体需要的铁元素,故答案为:②③;
(5)三大合成材料是塑料、合成纤维、合成橡胶,故答案为:③;
(6)碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,反应的离子方程式为:MgCO3+2H+═Mg2++CO2↑+H2O;氢氧化铝和盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3H+═Al3++3H2O,故答案为:MgCO3+2H+═Mg2++CO2↑+H2O;Al(OH)3+3H+═Al3++3H2O.
故答案为:还原;氧化;
(2))服用维生素C,可使食物中的Fe3+还原成Fe2+,说明维生素C具有还原性,在反应中为还原剂,被氧化,可用FeCl3溶液和KSCN溶液进行检验,在红色溶液中滴加维生素C,如溶液血红色褪去,说明维生素C具有还原性,能将Fe3+还原为Fe2+,维生素可根据其溶解性的不同分为脂溶性维生素和水溶性维生素,维生素C为水溶性维生素,故答案为:还原;先变红后褪色;水溶;脂溶;
(3)铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐的化学反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(4)铁是合成血红蛋白的主要元素,缺乏会患缺铁性贫血,酱油加铁可补充人体需要的铁元素,故答案为:②③;
(5)三大合成材料是塑料、合成纤维、合成橡胶,故答案为:③;
(6)碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,反应的离子方程式为:MgCO3+2H+═Mg2++CO2↑+H2O;氢氧化铝和盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3H+═Al3++3H2O,故答案为:MgCO3+2H+═Mg2++CO2↑+H2O;Al(OH)3+3H+═Al3++3H2O.
点评:本题考查氧化还原反应、离子方程式等知识,为高频考点,侧重于学生的分析能力的考查,题目注重基础,难度较小,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的具有的性质.

练习册系列答案
相关题目
下列各组物质中,依次属于单质、酸、盐的一组是( )
| A、干冰、石灰石、氧化钙 |
| B、氧气、氢氯酸、氯化铵 |
| C、水、烧碱、食盐 |
| D、氯水、硝酸、纯碱 |
下列叙述正确的是( )
| A、只有在标准状况下,48 g O3气体才含有6.02×1023个O3分子 |
| B、常温常压下,4.6 gNO2气体约含有1.81×1023个原子 |
| C、0.5 mol?L-1CuCl2溶液中含有Cu2+数小于3.01×1023个 |
| D、标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
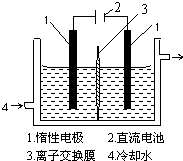 在全民补碘政策实施了15年之久的今天,有媒体报道称,一些地区的临床医生反映甲状腺疾病发病呈上升趋势,于是一些专家呼吁,停止对食盐进行国家的强制加碘,应该根据不同地区的实际情况来决定是否应该加碘.食盐加碘剂主要成份是碘酸钾(KIO3).工业上可用碘为原料通过电解制备碘酸钾.
在全民补碘政策实施了15年之久的今天,有媒体报道称,一些地区的临床医生反映甲状腺疾病发病呈上升趋势,于是一些专家呼吁,停止对食盐进行国家的强制加碘,应该根据不同地区的实际情况来决定是否应该加碘.食盐加碘剂主要成份是碘酸钾(KIO3).工业上可用碘为原料通过电解制备碘酸钾.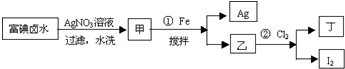
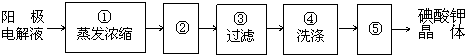
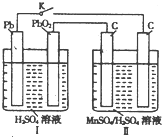 高锰酸钾和二氧化锰是中学化学常用的化学试剂.根据下面相关的信息回答下列问题:
高锰酸钾和二氧化锰是中学化学常用的化学试剂.根据下面相关的信息回答下列问题: