题目内容
除去下列括号中所有的杂质(括号内的物质),将选用的试剂填在横线上,并写出反应化学方程式:
(1)Fe2O3(Al2O3) ;方程式 ;
(2)Fe2O3(Fe(OH)3) ;方程式 ;
(3)Fe(Al) ;方程式 .
(1)Fe2O3(Al2O3)
(2)Fe2O3(Fe(OH)3)
(3)Fe(Al)
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:元素及其化合物,化学实验基本操作
分析:(1)Al2O3与NaOH溶液反应,而Fe2O3不能,则加足量NaOH溶解后过滤可除杂;
(2)Fe(OH)3加热分解生成Fe2O3;
(3)Al与NaOH溶液反应,而Fe不能,则加足量NaOH溶解后过滤可除杂.
(2)Fe(OH)3加热分解生成Fe2O3;
(3)Al与NaOH溶液反应,而Fe不能,则加足量NaOH溶解后过滤可除杂.
解答:
解:(1)Al2O3与NaOH溶液反应,而Fe2O3不能,则加足量NaOH溶解后过滤可除杂,则选择试剂为NaOH,发生的反应为Al2O3+2NaOH═2NaAlO2+H2O,
故答案为:NaOH;Al2O3+2NaOH═2NaAlO2+H2O;
(2)Fe(OH)3加热分解生成Fe2O3,则除杂方法为加热法,反应为2Fe(OH)3
Fe2O3+3H2O,故答案为:加热;2Fe(OH)3
Fe2O3+3H2O;
(3)Al与NaOH溶液反应,而Fe不能,则加足量NaOH溶解后过滤可除杂,选择试剂为NaOH,发生的离子反应为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案为:NaOH;2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
故答案为:NaOH;Al2O3+2NaOH═2NaAlO2+H2O;
(2)Fe(OH)3加热分解生成Fe2O3,则除杂方法为加热法,反应为2Fe(OH)3
| ||
| ||
(3)Al与NaOH溶液反应,而Fe不能,则加足量NaOH溶解后过滤可除杂,选择试剂为NaOH,发生的离子反应为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案为:NaOH;2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
点评:本题考查物质分离、提纯的方法及选择,为高频考点,把握物质的性质及分离方法为解答的关键,侧重除杂的考查,注意物质的性质差异及除杂原则,题目难度不大.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
在一定条件下体积不变的密闭容器中,一定量的混合气体发生反应:aA(g)+bB(g)?cC(g)△H<0,达到平衡时,测得c(B)=0.48mol?L-1.保持温度不变,把容器体积扩大到原来的2倍,使其重新达到平衡,测得c(B)=0.27mol?L-1.下列有关说法不正确的是( )
| A、a+b>c |
| B、A的转化率增大 |
| C、C的体积分数降低 |
| D、平衡一定逆向移动 |
 ⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.
⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.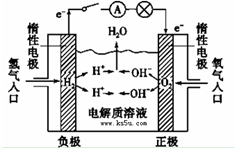 已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量.根据以上所给的数据计算反应:
已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量.根据以上所给的数据计算反应: “探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过.
“探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过. “神九”飞船的发射成功,标志着我国航天事业进入领先行业.
“神九”飞船的发射成功,标志着我国航天事业进入领先行业.