题目内容
5.下列说法中不正确的是( )| A. | 共价化合物中一定不含有离子键,离子化合物中可能含有共价键 | |
| B. | 充电电池的化学反应原理是氧化还原反应 | |
| C. | 一定条件下,将1 mol N2与3 mol H2充入密闭容器中充分反应可生成2 mol NH3 | |
| D. | 质子数相同、电子数也相同的两种微粒,不可能是一种分子和一种离子 |
分析 A.离子化合物中一定含有离子键,可能含有共价键;
B.充电电池的充电、放电过程都有电子得失,都是氧化还原反应,且是相互逆向进行的;
C.可逆反应不可能完全转化;
D.而离子中质子数和电子数一定是不相等的.
解答 解:A、含有离子键的化合物是离子化合物,全部由共价键形成的化合物是共价化合物,故A正确;
B、充电电池的化学反应有化合价的变化,所以是氧化还原反应,故B正确;
C、氨气的合成是可逆反应,转化率不可能是100%的,故C错误;
D、分子中质子数和电子数一定是相等,而离子中质子数和电子数一定是不相等的,所以不可能是离子,故D正确;
故选C.
点评 本题考查的概念较多,难度不大,注意基础知识的掌握,选项D学生要掌握质子数、中子数、质量数等的关系.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
15.不粘锅是在普通锅的内侧涂覆上一层树脂而成,这层树脂的主要成分是聚四氟乙烯.洗衣店干洗西装是用有机溶剂来洗衣服的,目前使用的标准干洗剂的主要成分是四氯乙烯.关于聚四氟乙烯和四氯乙烯,下面的说法正确的是( )
| A. | 它们都是乙烯的同系物 | B. | 它们都属于混合物 | ||
| C. | 它们的分子中都含有C=C双键 | D. | 它们分子中都不含氢原子 |
13.人的血液里Ca2+的浓度一般采用g•cm-3表示,今抽一血样20.00mL加入适量的草酸铵[(NH4)2C2O4]溶液,可析出CaC2O4沉淀,将沉淀洗净后溶于强酸可得草酸,再用浓度为0.02mol•L-1的KMnO4溶液滴定.当观察到溶液紫色褪尽时,共消耗12.00mL KMnO4溶液.则该血液样品中Ca2+的浓度为( )
| A. | 0.0015 g•cm-3 | B. | 0.0012 g•cm-3 | C. | 0.0024 g•cm-3 | D. | 0.002 g•cm-3 |
20.下列关于物质性质变化的比较,不正确的是( )
| A. | 非金属性强弱:I>Br>Cl | B. | 原子半径大小:Na>P>S | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
10.下列有关说法错误的是( )
| A. | 已知氯化钴及其水合物会呈现不同颜色(如下),德国科学家发明了添加氯化钴的变色水泥,据此推测雨天变色水泥呈粉红色 | |
| B. | 已知铬酸根(黄色)和重铬酸根(橙色)离子间存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O,若加水稀释,则溶液中所有离子浓度均减少 | |
| C. | 若反应2A(g)+B(s)?C(g)+3D(g)只有高温下才能自发进行,则该反应的△H>0 | |
| D. | 增大反应物的浓度,可使单位体积内活化分子数目增多,反应速率加快 |
14.关于下列各图的叙述,正确的是( )
| A. | 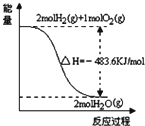 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为-241.8kJ•mol-1 | |
| B. | 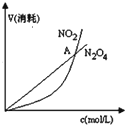 表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 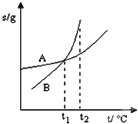 表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| D. | 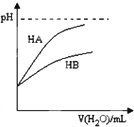 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化.则NaA溶液的pH小于等物质的量浓度的NaB溶液的pH |
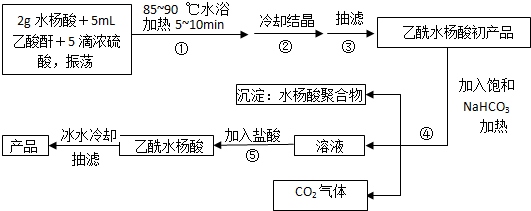
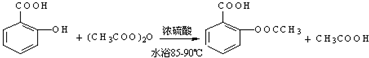 ;反应类型取代反应;
;反应类型取代反应; 、
、 ;
; ;
;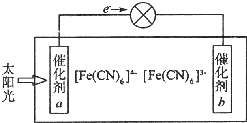 铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题. 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )