题目内容
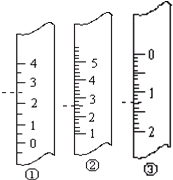 (1)如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是
(1)如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是温度计应该是
(2)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是
①用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡.
②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失
③中和滴定时,锥形瓶内有少量蒸馏水.
④酸式滴定管用蒸馏水洗后,未用标准液洗.
⑤读取滴定管终点读数时,仰视刻度线.
分析:(1)根据常见仪器的构造及图示液面位置进行解答;
(2)根据实验操作对c(待测)=
产生的影响进行分析误差.
(2)根据实验操作对c(待测)=
| c(标准)×V(标准) |
| V(待测) |
解答:解:(1)量筒没有0刻度,从下到上刻度增大,②为量筒,量筒读数读到0.1mL,图示液面读数为2.5mL;
滴定管零刻度在上方,③是滴定管,读数读到0.01mL,图示液面读数为1.30mL;
温度计零刻度以下有刻度,①应该是温度计,读数为2.5℃,
故答案为:②;2.5;③;1.30;①;2.5;
(2)①称量氢氧化钠时,配制的待测液氢氧化钠的浓度偏小,沉淀结果偏低,故①错误;
②滴定管尖嘴部分有气泡,滴定后消失,会导致测定标准液体积偏大,测定值偏高,故②正确;
③锥形瓶内有少量蒸馏水对待测液的物质的量没有影响,所以不影响测定结果,故③错误;
④酸式滴定管用蒸馏水润洗后,未用标准液润洗,造成V(标准)偏大,测定值偏高,故④正确;
⑤滴定终点读数时仰视读数,读出的标准溶液的体积偏大,则待测液浓度偏高,故⑤正确;
故答案为:②④⑤.
滴定管零刻度在上方,③是滴定管,读数读到0.01mL,图示液面读数为1.30mL;
温度计零刻度以下有刻度,①应该是温度计,读数为2.5℃,
故答案为:②;2.5;③;1.30;①;2.5;
(2)①称量氢氧化钠时,配制的待测液氢氧化钠的浓度偏小,沉淀结果偏低,故①错误;
②滴定管尖嘴部分有气泡,滴定后消失,会导致测定标准液体积偏大,测定值偏高,故②正确;
③锥形瓶内有少量蒸馏水对待测液的物质的量没有影响,所以不影响测定结果,故③错误;
④酸式滴定管用蒸馏水润洗后,未用标准液润洗,造成V(标准)偏大,测定值偏高,故④正确;
⑤滴定终点读数时仰视读数,读出的标准溶液的体积偏大,则待测液浓度偏高,故⑤正确;
故答案为:②④⑤.
点评:本题考查了中和滴定的误差分析、常见仪器的构造及使用方法,题目难度中等,注意掌握中和滴定的操作方法及误差分析的方法,熟悉常见计量仪器的构造及使用方法.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
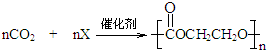 ,则X的结构简式为
,则X的结构简式为

 、
、 、
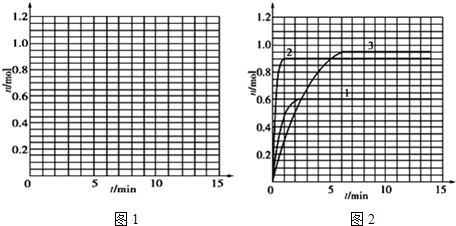
、 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是

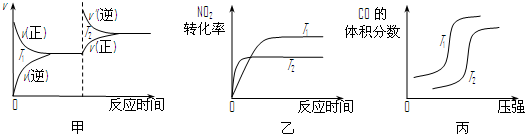
 的物质计量数;X1、X2表示不同温度或压强),某物理量Y随时间(t)变化的情况如图所示,
的物质计量数;X1、X2表示不同温度或压强),某物理量Y随时间(t)变化的情况如图所示,