题目内容
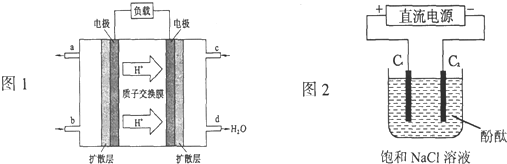
 如图是电解饱和食盐水的装置,下列有关判断正确的是( )
如图是电解饱和食盐水的装置,下列有关判断正确的是( )分析:由题意,碳棒与电源正极相连,做阳极,发生氧化反应,即:2Cl-=Cl2↑+2e-,碳棒周围生成的Cl2能氧化碘化钾生成碘,碳棒与电源负极相连做阴极,发生还原反应,即:2H++2e-=H2↑,周围溶液c(OH-)增大,碱性增强,滴加酚酞应该变红.
解答:解:A.因离子氧化性H+>Na+,阴极发生还原反应生成氢气,不可能生成Na,故A错误;
B.阴极发生2H++2e-=H2↑,促进水的电离,周围溶液c(OH-)增大,碱性增强,滴加酚酞应该变红,故B错误;
C.阳极发生氧化反应:2Cl-=Cl2↑+2e-,碳棒周围生成的Cl2能氧化碘化钾生成碘,溶液显棕黄色,故C正确;
D.电解过程中,阴极发生的是还原反应,故D错误.
故选C.
B.阴极发生2H++2e-=H2↑,促进水的电离,周围溶液c(OH-)增大,碱性增强,滴加酚酞应该变红,故B错误;
C.阳极发生氧化反应:2Cl-=Cl2↑+2e-,碳棒周围生成的Cl2能氧化碘化钾生成碘,溶液显棕黄色,故C正确;
D.电解过程中,阴极发生的是还原反应,故D错误.
故选C.
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,主要是考查学生对电解池的电极反应、现象和电极反应式的书写等的掌握情况,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力.该题的关键是明确电解的工作原理,然后灵活运用即可.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
 通过煤的气化和液化,使碳及其化合物得以广泛应用.
通过煤的气化和液化,使碳及其化合物得以广泛应用.I.工业上先用煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:CO(g)+H2O(g)?CO2(g)+H2(g)
(1)向1L恒容密闭容器中充人CO和H2O(g),800℃时测得部分数据如下表.
| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 0.600 | 0.520 | 0.450 | 0.350 | 0.350 |
| n(CO)/mol | 0.400 | 0.320 | 0.250 | 0.150 | 0.150 |
(2)相同条件下,向2L恒容密闭容器中充入1mol CO、1mol H2O(g)、2mol CO2、2mol H2,此时υ(正)
Ⅱ.已知CO(g)、H2(g)、CH3OH(l)的燃烧热分别为283kJ?mol-1、286kJ?mol-1、726kJ?mol-1.
(3)利用CO、H2合成液态甲醇的热化学方程式为
(4)依据化学反应原理,分析增加压强对制备甲醇反应的影响
Ⅲ.为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作原理如图所示:一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.
(5)以辛烷(C8H18)代表汽油,写出该电池工作时的负极反应方程式
(6)已知一个电子的电量是1.602×10-19C,用该电池电解饱和食盐水,当电路中通过1.929×105C的电量时,生成NaOH
Ⅳ.煤燃烧产生的CO2是造成温室效应的主要气体之一.
(7)将CO2转化成有机物可有效地实现碳循环.如:
a.6CO2+6H2O
| 光照/叶绿素 |
b.2CO2+6H2
| ||
| △ |
c.CO2+CH4
| ||
| △ |
d.2CO2+6H2
| ||
| △ |
以上反应中,最节能的是