题目内容
 通过煤的气化和液化,使碳及其化合物得以广泛应用.
通过煤的气化和液化,使碳及其化合物得以广泛应用.I.工业上先用煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:CO(g)+H2O(g)?CO2(g)+H2(g)
(1)向1L恒容密闭容器中充人CO和H2O(g),800℃时测得部分数据如下表.
| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 0.600 | 0.520 | 0.450 | 0.350 | 0.350 |
| n(CO)/mol | 0.400 | 0.320 | 0.250 | 0.150 | 0.150 |
(2)相同条件下,向2L恒容密闭容器中充入1mol CO、1mol H2O(g)、2mol CO2、2mol H2,此时υ(正)
Ⅱ.已知CO(g)、H2(g)、CH3OH(l)的燃烧热分别为283kJ?mol-1、286kJ?mol-1、726kJ?mol-1.
(3)利用CO、H2合成液态甲醇的热化学方程式为
(4)依据化学反应原理,分析增加压强对制备甲醇反应的影响
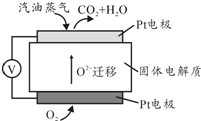
Ⅲ.为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作原理如图所示:一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.
(5)以辛烷(C8H18)代表汽油,写出该电池工作时的负极反应方程式
(6)已知一个电子的电量是1.602×10-19C,用该电池电解饱和食盐水,当电路中通过1.929×105C的电量时,生成NaOH
Ⅳ.煤燃烧产生的CO2是造成温室效应的主要气体之一.
(7)将CO2转化成有机物可有效地实现碳循环.如:
a.6CO2+6H2O
| 光照/叶绿素 |
b.2CO2+6H2
| ||
| △ |
c.CO2+CH4
| ||
| △ |
d.2CO2+6H2
| ||
| △ |
以上反应中,最节能的是
分析:I.(1)化学平衡常数为平衡时,生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值;
(2)温度不变,利用浓度商与化学平衡常数的大小,判断平衡移动方向,得到答案;
Ⅱ.(3)根据CO和CH3OH的燃烧热先书写热方程式,再利用盖斯定律来分析甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式;
(4)分析压强对化学反应速率和化学平衡的影响,得到答案;
(5)电解质能在高温下能传导O2-,负极发生氧化反应,即C8H18)失去电子生成CO2,根据质量守恒和电荷守恒写出电极反应式;
(6)一个电子的电量是1.602×10-19C,当电路中通过1.929×105 C的电量时,电子的个数=
=1.204×1024,电子的物质的量=
=
2mol,根据转移电子和氢氧化钠的关系式计算;
(7)最节能的措施应使用太阳能;原子利用率等于期望产物的总质量与生成物的总质量之比.
(2)温度不变,利用浓度商与化学平衡常数的大小,判断平衡移动方向,得到答案;
Ⅱ.(3)根据CO和CH3OH的燃烧热先书写热方程式,再利用盖斯定律来分析甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式;
(4)分析压强对化学反应速率和化学平衡的影响,得到答案;
(5)电解质能在高温下能传导O2-,负极发生氧化反应,即C8H18)失去电子生成CO2,根据质量守恒和电荷守恒写出电极反应式;
(6)一个电子的电量是1.602×10-19C,当电路中通过1.929×105 C的电量时,电子的个数=
| 1.929×105C |
| 1.602×10-19C |
| 1.204×1024 |
| 6.02×1023mol-1 |
2mol,根据转移电子和氢氧化钠的关系式计算;
(7)最节能的措施应使用太阳能;原子利用率等于期望产物的总质量与生成物的总质量之比.
解答:解:I.(1)反应物和生成物浓度不变时,达到平衡状态,3min后达到平衡状态,容器体积为1L,则c(H2O)=0.350mol/L,c(CO)=0.150mol/L,c(H2)=c(CO2)=
0.600mol/L-0.350mol/L=0.250mol/L,化学平衡常数表达式为:K=
=
=1.2,故答案为:1.2;
(2)向2L恒容密闭容器中充入1mol CO、1mol H2O(g)、2mol CO2、2mol H2,各物质浓度分别为:0.5mol/L、0.5mol/L、1mol/L、1mol/L,浓度商=
=4>1.2,平衡向逆反应方向移动,所以υ(正)<υ(逆),故答案为:<;
Ⅱ.(3)由CO(g)和CH3OH(l)的燃烧热△H分别为-283.0kJ?mol-1和-726.5kJ?mol-1,则
①CO(g)+
O2(g)=CO2(g)△H=-283.0kJ?mol-1
②CH3OH(l)+
O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ?mol-1
③H2(g)+
O2(g)=H2O(l)△H=-286kJ?mol-1
由盖斯定律可知用①+③-
×②得反应CO(g)+2H2(g)=CH3OH(l),该反应的反应热△H═-283.0kJ?mol-1+(-286kJ?mol-1)-
×(-726.5kJ?mol-1)=-129kJ?mol-1,CO(g)+2H2(g)=CH3OH(l)△H=-129kJ?mol-1
故答案为:CO(g)+2H2(g)=CH3OH(l)△H=-129kJ?mol-1;
(4)增加压强,缩小体积,反应物浓度增大,反应速率加快,正反应速率加快大于逆反应速率,化学平衡向正反应方向移动,故答案为:增加压强使反应速率加快,同时平衡右移,CH3OH产率增大;
(5)电解质能在高温下能传导O2-,负极发生氧化反应,即1molC8H18失去电子生成CO2,共失去8×[+4-(-
)]=50mole-,18molH原子转化为9molH2O,根据质量守恒和电荷守恒写出电极反应为:C8H18-50e-+25O2-=8CO2+9H2O,故答案为:C8H18-50e-+25O2-=8CO2+9H2O;
(6)一个电子的电量是1.602×10-19C,当电路中通过1.929×105 C的电量时,电子的个数=
=1.204×1024,电子的物质的量=
=2mol,根据转移电子和氢氧化钠的关系式得NaOH的质量=
×2×40g?mol-1=80g,故答案为80;
(7)最节能的措施应使用太阳能;原子利用率等于期望产物的总质量与生成物的总质量之比,反应b中理论上原子利用率为:
×100%,
故答案为:a、46%.
0.600mol/L-0.350mol/L=0.250mol/L,化学平衡常数表达式为:K=
| [CO2]?[H2] |
| [CO]?[H2O] |
| 0.250×0.250 |
| 0.350×0.150 |
(2)向2L恒容密闭容器中充入1mol CO、1mol H2O(g)、2mol CO2、2mol H2,各物质浓度分别为:0.5mol/L、0.5mol/L、1mol/L、1mol/L,浓度商=
| 1×1 |
| 0.5×0.5 |
Ⅱ.(3)由CO(g)和CH3OH(l)的燃烧热△H分别为-283.0kJ?mol-1和-726.5kJ?mol-1,则
①CO(g)+
| 1 |
| 2 |
②CH3OH(l)+
| 3 |
| 2 |
③H2(g)+
| 1 |
| 2 |
由盖斯定律可知用①+③-
| 2 |
| 3 |
| 2 |
| 3 |
故答案为:CO(g)+2H2(g)=CH3OH(l)△H=-129kJ?mol-1;
(4)增加压强,缩小体积,反应物浓度增大,反应速率加快,正反应速率加快大于逆反应速率,化学平衡向正反应方向移动,故答案为:增加压强使反应速率加快,同时平衡右移,CH3OH产率增大;
(5)电解质能在高温下能传导O2-,负极发生氧化反应,即1molC8H18失去电子生成CO2,共失去8×[+4-(-
| 18 |
| 8 |
(6)一个电子的电量是1.602×10-19C,当电路中通过1.929×105 C的电量时,电子的个数=
| 1.929×105C |
| 1.602×10-19C |
| 1.204×1024 |
| 6.02×1023mol-1 |
| 2mol |
| 2 |
(7)最节能的措施应使用太阳能;原子利用率等于期望产物的总质量与生成物的总质量之比,反应b中理论上原子利用率为:
| 46 |
| 88+12 |
故答案为:a、46%.
点评:本题考查影响化学平衡的因素、化学平衡的建立等,难度较大,构建平衡建立的途径进行比较是关键;探讨了能源的循环利用和温室效应的解决,着重考查了物质催化反应的过程,结合考查了化学反应速率和对图表的理解解析能力,综合能力要求较高.另外读图时要注意观察横纵坐标的含义和单位.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
下列与能源及利用有关的描述中,不正确的是( )
| A、化学物质发生反应放热或吸热由反应物和生成物的总能量决定 | B、可通过将煤粉碎等措施提高煤燃烧效率 | C、核能利用有可能造成辐射危害,故应限制其发展 | D、煤的气化和液化是高效、清洁地利用煤炭的重要途径 |