题目内容
将两种硫酸盐按一定比例混合后共熔,可制得化合物x,x溶于水能电离出K+离子、Cr3+和若向溶有2.839 gx的溶液中加入过量的BaCl2溶液,可得到4.66 g沉淀,由此可推断x的化学式为( )
A.K2SO4·2Cr2(SO4)3 B.2K2SO4·Cr2(SO4)3
C.K2SO4·Cr2(SO4)3 D.K2SO4·0.5Cr2(SO4)3
答案:C
解析:
解析:
| 解析:依题意有2Cr ~ 3I2由此求出n(Cr)=0.01 mol n(SO42-)=0.02 mol 即n(Cr)∶n(
|

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
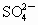 离子,现将2.83g W中的Cr3+离子全部氧化成
离子,现将2.83g W中的Cr3+离子全部氧化成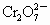 离子,再和过量KI溶液反应(
离子,再和过量KI溶液反应(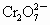 +6I-+14H+
+6I-+14H+ 2Cr3++3I2+7H2O)得到3.81g I2,另取2.83g W投入过量BaCl2溶液中,得到4.66g沉淀,由此判断W的化学式为:
2Cr3++3I2+7H2O)得到3.81g I2,另取2.83g W投入过量BaCl2溶液中,得到4.66g沉淀,由此判断W的化学式为: ,现将2.83g W中的Cr3+全部氧化为
,现将2.83g W中的Cr3+全部氧化为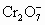 后,这些
后,这些