题目内容
某溶液中可能含有下列6种离子中的某几种:Cl—、SO42— 、CO32—、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
、CO32—、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
A.一定存在SO42—、CO32—、NH4+,可能存在Cl—、Na+、K+
B.一定存在Cl—、SO42—、CO32—、NH4+,一定不存在Na+、K+
C.原溶液中c(CO32—)=0.01mol·L-1
D.如果上述6种离子都存在,则c(Cl—)>c(SO42—)
练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2.下列实验能达到测量要求的是( )
| A. | 用托盘天平称取35.20g NaCl固体 | |
| B. | 用25mL酸式滴定管量取15.80mL盐酸溶液 | |
| C. | 用10mL量筒量取8.50mL盐酸 | |
| D. | 用广泛pH试纸测得某溶液pH值为4.2 |
3.下列各组离子能够在指定环境下大量共存的是( )
| A. | 在pH=0的溶液中:Na+、K+、MnO4-、Cl- | |
| B. | 和Al反应能产生H2的溶液:K+、NH4+、Cl-、S2O32- | |
| C. | 中性溶液:Al3+、K+、SO42-、AlO2- | |
| D. | c(H+)<c(OH-)的溶液:Na+、K+、SO32-、S2- |
6.下列反应的离子方程式书写正确的是( )
| A. | 金属钠投入到足量的稀盐酸中:Na+2H+=Na++H2↑ | |
| B. | CuO溶解在稀盐酸中:O-+2H+=H2O | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O | |
| D. | 碳酸氢钙溶液与稀盐酸反应:HCO3-+H+=H2O+CO2↑ |
7.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 含1molFeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 1 ml的水分子与1 mol的氢氧根离子所含电子数均为10NA | |
| C. | 常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA | |
| D. | 在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA |


 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,正确的是( )
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,正确的是( )
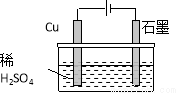
 CuSO4+H2↑
CuSO4+H2↑ 板:2Fe3++Cu=2Fe2++Cu2+
板:2Fe3++Cu=2Fe2++Cu2+