题目内容
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4L甲烷和乙炔混合气体所含的分子数为NA |
| B、12g NaHSO4晶体中含有H+离子数为0.1NA |
| C、60g乙酸分子中含共价键总数为6NA |
| D、11.2L Cl2与足量的NaOH溶液反应转移的电子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,22.4L甲烷和乙炔的混合气体的物质的量为1mol;
B.硫酸氢钠晶体中不存在氢离子,存在是钠离子和硫酸氢根离子;
C.乙酸分子的结构式为: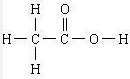 ,乙酸中含有6个单键和1个碳氧双键,总共含有8个共价键;
,乙酸中含有6个单键和1个碳氧双键,总共含有8个共价键;
D.没有告诉在标况下,题中条件无法计算11.2L氯气的物质的量.
B.硫酸氢钠晶体中不存在氢离子,存在是钠离子和硫酸氢根离子;
C.乙酸分子的结构式为:
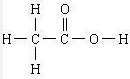 ,乙酸中含有6个单键和1个碳氧双键,总共含有8个共价键;
,乙酸中含有6个单键和1个碳氧双键,总共含有8个共价键;D.没有告诉在标况下,题中条件无法计算11.2L氯气的物质的量.
解答:
解:A.标准状况下,22.4L甲烷和乙炔混合气体的物质的量为1mol,所含的分子数为NA,故A正确;
B.12g NaHSO4晶体的物质的量为0.1mol,0.1mol硫酸氢钠中含有0.1mol钠离子和0.1mol硫酸氢根离子,不存在氢离子,故B错误;
C.60g乙酸的物质的量为1mol,根据乙酸的结构式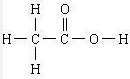 可知:乙酸官能团为羧基-COOH,1 mol 分子中含有碳氢单键为4 mol,含碳碳单键为1 mol,含碳氧双键为1 mol,1 mol碳氧双键含2mol共价键,含碳氧单键为1 mol,所以1 mol乙酸分子中共价键总数为8NA,故C错误;
可知:乙酸官能团为羧基-COOH,1 mol 分子中含有碳氢单键为4 mol,含碳碳单键为1 mol,含碳氧双键为1 mol,1 mol碳氧双键含2mol共价键,含碳氧单键为1 mol,所以1 mol乙酸分子中共价键总数为8NA,故C错误;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算氯气的物质的量,故D错误;
故选A.
B.12g NaHSO4晶体的物质的量为0.1mol,0.1mol硫酸氢钠中含有0.1mol钠离子和0.1mol硫酸氢根离子,不存在氢离子,故B错误;
C.60g乙酸的物质的量为1mol,根据乙酸的结构式
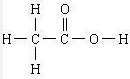 可知:乙酸官能团为羧基-COOH,1 mol 分子中含有碳氢单键为4 mol,含碳碳单键为1 mol,含碳氧双键为1 mol,1 mol碳氧双键含2mol共价键,含碳氧单键为1 mol,所以1 mol乙酸分子中共价键总数为8NA,故C错误;
可知:乙酸官能团为羧基-COOH,1 mol 分子中含有碳氢单键为4 mol,含碳碳单键为1 mol,含碳氧双键为1 mol,1 mol碳氧双键含2mol共价键,含碳氧单键为1 mol,所以1 mol乙酸分子中共价键总数为8NA,故C错误;D.不是标准状况下,不能使用标况下的气体摩尔体积计算氯气的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项B为易错点,注意硫酸氢钠中不存在氢离子.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
有两种不同的原子团-X、-Y,若同时分别取代甲苯苯环上的两个氢原子,生成的同分异体的数目是( )
| A、10种 | B、9种 | C、6种 | D、4种 |
 如图所示,将紧紧缠绕不同金属丝的铁钉放入培养皿中,再加入含有适量NaCl的溶液.下列叙述正确的是( )
如图所示,将紧紧缠绕不同金属丝的铁钉放入培养皿中,再加入含有适量NaCl的溶液.下列叙述正确的是( )| A、a中铜丝上发生氧化反应 |
| B、b中铁钉上发生还原反应 |
| C、a、b中的铁钉均会发生锈蚀 |
| D、a、b中反应时均有氢气放出 |
 为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )
为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )| A、左边铜片上有气泡冒出 |
| B、右边锌片上的反应为2Cl--2e-=Cl2↑ |
| C、最先观察到红色的区城是② |
| D、左右两边Cu片质量均不发生变化 |
下列物质的水溶液中只存在一种分子的是( )
| A、Na2SO4 |
| B、NaHS |
| C、HNO3 |
| D、HClO |
下列各组离子中,在指定溶液中一定能大量存在的是( )
| A、澄清透明的无色溶液:ClO-、MnO4-、Al3+、SO42- |
| B、含有大量Fe3+的溶液:H+、I-、K+、Cl- |
| C、能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- |
| D、由水电离产生的c(H+)=1×10-12mol/L的溶液:NH4+、Na+、Cl-、HCO3- |
实验室保存下列药品的方法,正确的是( )
| A、氢氟酸贮存在细口玻璃瓶里 |
| B、盛溴的试剂瓶里加一些水来防止溴挥发 |
| C、盛放浓硫酸的广口瓶应当用磨口玻璃塞,不能用橡皮塞 |
| D、氯水保存在无色玻璃瓶中;液氯存贮存在钢瓶里 |
下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是( )
| A、SO2、H2S、Cl2 |
| B、SO2、O2、NH3 |
| C、SO2、CO2、O2 |
| D、HCl、H2S、HI |