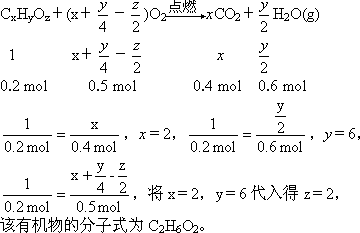题目内容
0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).燃烧后的这些产物经过浓H2SO4后,质量增加10.8 g;再通过灼热的CuO充分反应后,固体质量减轻3.2 g,最后气体再通过碱石灰被完全吸收,质量增加17.6 g.
(1)推断该有机物的分子式.
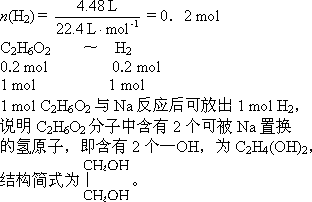
(2)若0.2 mol该有机物在与过量的金属钠完全反应后放出4.48 L H2(标准状况),试确定有机物的结构简式.
答案:
解析:
解析:
|
答案:(1)C2H6O2 (2) 解析:①浓H2SO4增重说明生成水的质量为10.8 g.②灼热的CuO减重3.2 g,说明生成的CO被氧化为CO2,故碱石灰增重实际为原燃烧生成的CO2及CO被氧化生成的CO2质量之和.③该物质与金属钠能发生反应产生H2,说明含有-OH,这是推断其结构的依据.④O2的量不足量. 根据条件: (1)燃烧产物中有CO,说明有机物燃烧时O2不足.CO通过灼热的CuO充分反应后,CuO质量减轻3.2 g,即参与反应的CuO中含氧元素3.2 g,也就是有机物燃烧时缺少O2的质量为3.2 g.3.2 g O2的物质的量为 n(CO2)= 设该有机物的分子式为CxHyOz. (2)可与Na反应放出H2,说明其结构中含有羟基(-OH). |

练习册系列答案
相关题目