题目内容
5.物质的量浓度、体积都相同的NaF和NaCN溶液中,离子总数的关系正确的是(已知HF比HCN易电离)( )| A. | NaF=NaCN | B. | NaF>NaCN | C. | NaF<NaCN | D. | 无法确定 |
分析 已知HF比HCN易电离,则等体积、等浓度的NaF和NaCN溶液中CN-水解程度更大,结合溶液电荷守恒判断.
解答 解:根据电荷守恒,c(F-)+c(OH-)=c(Na+)+c(H+),c(CN-)+c(OH-)=c(Na+)+c(H+),即离子总数是n(Na+ )+n(H+)的2倍,
而NaCN的水解程度大,即NaCN溶液中的c(OH-)大,c(H+)小,c(Na+)相同,所以氟化钠中离子浓度大,
故选B.
点评 本题考查盐类的水解,为高频考点,侧重于学生的分析能力的考查,注意把握水解的程度,从溶液电中性的角度解答该题,难度中等.

练习册系列答案
相关题目
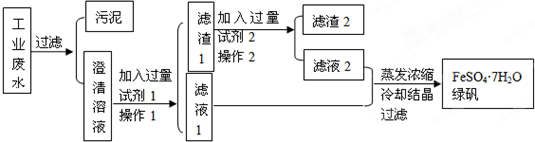
15.某同学在探究废干电池内的黑色固体回收利用时,进行如下所示实验:

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2和石墨粉等物质.请回答以下问题:
(1)操作②玻璃棒的作用是引流;操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、坩埚 和三脚架;
(2)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(填化学式).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2(填化学式).
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2和石墨粉等物质.请回答以下问题:
(1)操作②玻璃棒的作用是引流;操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、坩埚 和三脚架;
(2)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(填化学式).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2(填化学式).
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 有白色沉淀产生 | 含有Cl- |
| 2检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ |
20.下列说法不正确的是( )
| A. | 正常雨水的pH为7.0,酸雨的pH小于7.0 | |
| B. | 严格执行机动车尾气排放标准有利于防止大气污染 | |
| C. | 使用二氧化硫和某些含硫化合物漂白食品会对人体健康产生危害 | |
| D. | 使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害 |
10.一种无色气体100mL,由NH3、NO、CO2所组成,将此无色气体通过浓硫酸的洗气瓶后,发现气体减少了30mL.剩余气体继续通过Na2O2固体后,发现气体变成红棕色,再将该气体通入盛满水倒立于水槽中的试管内,发现试管内水位上升,最后试管内充满液体.则原混合气体中NH3、NO、CO2气体的体积比为( )
| A. | 5:8:12 | B. | 15:14:21 | C. | 10:14:21 | D. | 30:28:23 |
17.下列说法正确的是( )
| A. | 乙醇易溶于水,难溶于有机溶剂 | |
| B. | 苯的分子结构中含有碳碳双键 | |
| C. | 乙烯通入酸性KMn04溶液中,紫色褪去 | |
| D. | 苯的硝化、乙烯使高锰酸钾酸性溶液褪色的反应都属于取代反应 |
14.下列实验基本操作及注意事主要出于安全考虑的是( )
| A. | 实验剩余的药品不能放回原试剂瓶 | B. | 酒精灯内酒精不能少于灯容积$\frac{1}{4}$ | ||
| C. | 实验结束后将试管清洗干净 | D. | 胶头滴管不能交叉使用 |
15.不能用有关胶体的观点解释的现象是( )
| A. | 在江河入海处易形成三角洲 | |
| B. | 向污水加入适量的明矾,可以使水变得澄清 | |
| C. | 在NaCl溶液中滴入AgNO3溶液,产生白色沉淀 | |
| D. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 |