题目内容
温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率大于80%
CD
【解析】
试题分析:A.反应在前50 s的平均速率为v(PCl3)=(0.16mol÷2.0L)÷50 s=0.0016mol/(L·s);错误;B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol/L>0.20mol÷2.0L =0.10mol/L,说明升高温度,平衡正向移动,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,正反应方向是吸热反应,则反应的△H>0,错误;C.在相同温度下,若起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,则反应正向进行,在达到平衡前v(正)>v(逆),正确;D.在温度不变时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g)  PCl3(g)+Cl2(g)经一段时间后达到平衡的等效开始状态是1mol PCl3、1.0molCl2,由于平衡时PCl3的物质的量是0.2mol, PCl3的转化率是80%;而在相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,相当与给体系增大压强,增大压强,平衡向气体体积减小的逆反应方向移动,所以达到平衡时,PCl3的转化率大于80%,正确。
PCl3(g)+Cl2(g)经一段时间后达到平衡的等效开始状态是1mol PCl3、1.0molCl2,由于平衡时PCl3的物质的量是0.2mol, PCl3的转化率是80%;而在相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,相当与给体系增大压强,增大压强,平衡向气体体积减小的逆反应方向移动,所以达到平衡时,PCl3的转化率大于80%,正确。
考点:考查化学反应速率的计算、反应热的判断、反应进行的方向及物质的平衡含量的计算的知识。

 名校课堂系列答案
名校课堂系列答案相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4 B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③ D.N2的转化率:②>①>③
 ,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。
,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。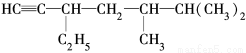 的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。
的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。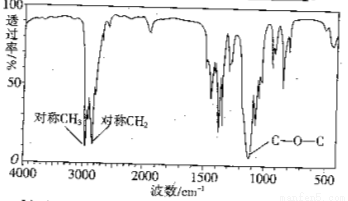
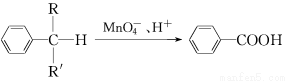
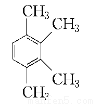 、 、 、 。
、 、 、 。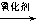 RCOOH+R,COOH。写出
RCOOH+R,COOH。写出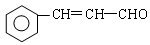 在强氧化剂条件下生成
在强氧化剂条件下生成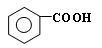 和另一种有机物 (写出其结构简式)。
和另一种有机物 (写出其结构简式)。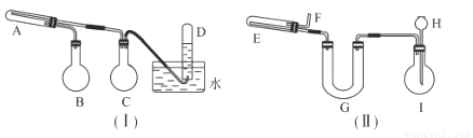

 。下列说法正确的是
。下列说法正确的是