题目内容
化学反应C(s)+H2O(g)?CO(g)+H2(g)在密闭容器中进行,下列改变可增大化学反应速率的是( )
| A、容器的体积缩小一半 |
| B、保持体积不变,充入氮气 |
| C、保持压强不变,充入氮气 |
| D、加入固体炭 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:A、体积缩小,反应体系中物质的浓度增大,相当于压强增大;
B、体积不变,反应体系中的各物质的浓度不变;
C、压强不变,充入N2,容器的体积变大,反应体系中各物质的浓度减小;
D、改变纯固体或液体的量,对反应速率无影响.
B、体积不变,反应体系中的各物质的浓度不变;
C、压强不变,充入N2,容器的体积变大,反应体系中各物质的浓度减小;
D、改变纯固体或液体的量,对反应速率无影响.
解答:
解:A、将容器的体积缩小一半,反应体系中物质的浓度增大,则化学反应速率增大,故A正确;
B、保持体积不变,充入N2,氮气不参与反应,反应体系中的各物质的浓度不变,则反应速率不变,故B错误;
C、保持压强不变,充入N2,使容器的体积变大,反应体系中各物质的浓度减小,则反应速率减小,故C错误;
D、因该反应中只有C为纯固体,则增加C的量对化学反应速率无影响,故D错误;
故选A.
B、保持体积不变,充入N2,氮气不参与反应,反应体系中的各物质的浓度不变,则反应速率不变,故B错误;
C、保持压强不变,充入N2,使容器的体积变大,反应体系中各物质的浓度减小,则反应速率减小,故C错误;
D、因该反应中只有C为纯固体,则增加C的量对化学反应速率无影响,故D错误;
故选A.
点评:本题考查增大化学反应速率的措施,明确常见的温度、浓度、压强、稀有气体等对化学反应速率的影响即可解答,抓住浓度是否变化来分析是关键.

练习册系列答案
相关题目
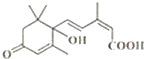 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、分子式为C15H22O4 |
| B、1mol该物质最多可以消耗H2和Br2的量分别为4mol和3mol |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、该物质可以发生分子内酯化反应形成六元环,也可以发生缩聚反应和加聚反应 |
下列说法中正确的是( )
| A、p轨道之间以“肩并肩”重叠可形成σ键 |
| B、p轨道之间以“头碰头”重叠可形成π键 |
| C、s和p轨道以“头碰头”重叠可形成σ键 |
| D、共价键是两个原子轨道以“头碰头”重叠形成的 |
下列实验中,不能观察到明显的变化的是( )
| A、把氯气通入FeCl3溶液中 |
| B、把绿豆大的钾投入水中 |
| C、把溴水滴加到KI淀粉溶液中 |
| D、把一段打磨过的镁带放入少量稀盐酸中 |
短周期元素X、Y、Z在周期表中的位置关系如图所示,下列叙述中正确的是( )
| X | ||
| Y | ||
| Z |
| A、Z一定是活泼金属元素 |
| B、X的最高价氧化物的水化物是一种强酸 |
| C、1molY的单质跟足量水反应时,发生转移的电子为1mol |
| D、Z的最高化合价为+6价 |
下列物质分离或提纯的方法,属于化学方法的是( )
| A、蒸馏使沸点低液体蒸出 |
| B、过滤除去不溶性杂质 |
| C、加热使杂质分解成气体 |
| D、萃取分液使溶质转移到另一溶剂中 |
如图所示,各烧杯中均盛有海水,铁在其中被腐蚀最快的为( )
A、 |
B、 |
C、 |
D、 |
下列对化学反应的认识错误的是( )
| A、必然伴随着能量的变化 |
| B、必然会产生新的物质 |
| C、必然会引起化学键的断裂 |
| D、必然引起物质状态的变化 |
下列热化学方程式表达正确的是(△H的绝对值均正确)( )
| A、S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol (反应热) |
| B、2NO2=O2+2NO△H=+116.2kJ/mol (反应热) |
| C、C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) |
| D、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=+57.3kJ/mol(中和热) |