题目内容
17.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )| A. | NaOH(固体) | B. | H2O | C. | NH4Cl(固体) | D. | CH3COOH |
分析 Fe过量,为了减缓反应速率,且不影响生成氢气的总量,可减小氢离子的浓度,但不能改变氢离子的物质的量,以此来解答
解答 解:Fe与盐酸反应的实质为Fe+2H+═Fe2++H2↑,为了减缓反应速度,且不影响生成氢气的总量,则可减小氢离子的浓度,但不改变氢离子的物质的量.
A、加入NaOH固体,氢离子的物质的量及浓度均减小,故A错误;
B、加入H2O,减小氢离子的浓度,但不改变氢离子的物质的量,故B正确;
C、加入NH4Cl固体,氢离子的浓度、氢离子的物质的量都没有明显变化,故C错误;
D、加入CH3COOH氢离子的物质的量增大,故D错误;
故选B.
点评 本题考查影响反应速率的因素,为高考常考考点,注意Fe过量,生成氢气由盐酸决定,把握浓度对反应速率的影响即可解答,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
8.表是周期表中的一部分,根据A-I在周期表中的位置,用元素符合或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ar,可用于制半导体材料的元素是Si.
(2)B的简单阳离子结构示意图为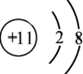 .
.
(3)在B、C、D、E、F中,原子半径最大的是Na.
(4)A分别与D、E、G形成的化合物中,最稳定的HF.
(5)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4.呈两性的是Al(OH)3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)B的简单阳离子结构示意图为
 .
.(3)在B、C、D、E、F中,原子半径最大的是Na.
(4)A分别与D、E、G形成的化合物中,最稳定的HF.
(5)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4.呈两性的是Al(OH)3.
5.有下列物质:(1)乙醇 (2)苯酚 (3)乙醛 (4)丙烯酸 (5)乙酸乙酯.其中与溴水、KMnO4酸性溶液、Na2CO3溶液都能反应的是( )
| A. | (1)(4) | B. | (2)(4) | C. | (4) | D. | (3)(4)(5) |
9.可以用分液漏斗进行分离的混合物是( )
| A. | 酒精和碘水 | B. | 苯和水 | C. | 乙酸和乙酸乙酯 | D. | 乙醇和水 |
6.现有部分元素的性质与原子(或分子)结构如下表:
(1)写出元素T的原子结构示意图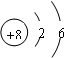 ;
;
(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是bd(填序号);
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(3)写出由Y元素最高价氧化物对应的水化物的电子式 ;
;
(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式N2H4+2H2O2═N2+4H2O.
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
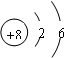 ;
;(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是bd(填序号);
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(3)写出由Y元素最高价氧化物对应的水化物的电子式
 ;
;(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式N2H4+2H2O2═N2+4H2O.
7.下列化合物中,含有共价键的离子化合物是( )
| A. | Na2S | B. | CaCl2 | C. | NaOH | D. | SO2 |
 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.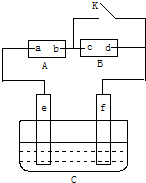 如图,A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图,A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:

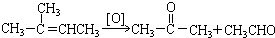
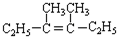 在上述类似条件下发生反应,请写出反应的方程式
在上述类似条件下发生反应,请写出反应的方程式 .
.