题目内容
 用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )
用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )| A、上下移动①中铜丝可控制反应开始停止 |
| B、若②中是澄清石灰水,先浑浊后澄清 |
| C、③中KMnO4溶液褪色,说明SO2有还原性 |
| D、①中铜丝换成光亮的铁丝,则因铁丝钝化而无明显现象 |
考点:浓硫酸的性质
专题:氧族元素
分析:A.Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,当铜和浓硫酸接触时才能生成二氧化硫;
B.二氧化硫和氢氧化钙反应先生成亚硫酸钙沉淀,亚硫酸钙和二氧化硫、水反应生成可溶性的亚硫酸氢钙;
C.二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化;
D.加热条件下,铁和浓硫酸发生氧化还原反应.
| ||
B.二氧化硫和氢氧化钙反应先生成亚硫酸钙沉淀,亚硫酸钙和二氧化硫、水反应生成可溶性的亚硫酸氢钙;
C.二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化;
D.加热条件下,铁和浓硫酸发生氧化还原反应.
解答:
解:A.当铜丝与浓硫酸接触时才能反应,当往上抽动铜丝时,铜丝与硫酸不接触,反应停止,故可通过上下移动①中铜丝可控制SO2的量,故A正确;
B.SO2+Ca(OH)2=CaSO3↓+H2O、CaSO3+SO2+H2O=Ca(HSO3)2,所以若②中是澄清石灰水,先浑浊后澄清,故B正确;
C.酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质,如果将二氧化硫通入酸性高锰酸钾溶液中,酸性高锰酸钾溶液褪色,则说明二氧化硫具有还原性,故C正确;
D.加热条件下,铁和浓硫酸反应生成硫酸铁、二氧化硫和水,所以有明显现象,故D错误;
故选D.
B.SO2+Ca(OH)2=CaSO3↓+H2O、CaSO3+SO2+H2O=Ca(HSO3)2,所以若②中是澄清石灰水,先浑浊后澄清,故B正确;
C.酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质,如果将二氧化硫通入酸性高锰酸钾溶液中,酸性高锰酸钾溶液褪色,则说明二氧化硫具有还原性,故C正确;
D.加热条件下,铁和浓硫酸反应生成硫酸铁、二氧化硫和水,所以有明显现象,故D错误;
故选D.
点评:本题考查二氧化硫的制备和性质,注意A为二氧化硫的简易制备方法,注意D中加热条件下铁和浓硫酸反应,常温下冷的浓硫酸和铁发生钝化,为易错点.

练习册系列答案
相关题目
甲基环己烷( )的一氯代物有( )
)的一氯代物有( )
 )的一氯代物有( )
)的一氯代物有( )| A、3种 | B、4种 | C、5种 | D、6种 |
用氢氧化钠固体配制一定物质的量浓度的氢氧化钠溶液,下列情况使溶液浓度偏高的是( )
| A、所用氢氧化钠中混有氧化钠 |
| B、用托盘天平称取一定质量的氢氧化钠时,所用的小烧杯内壁不太干燥 |
| C、向容量瓶中加水超过刻度线 |
| D、最后确定氢氧化钠溶液的体积(定容)时,仰视观察容量瓶刻度线 |
下列实验操作或装置不能达到目的是( )
A、 稀释浓硫酸 |
B、 分液 |
C、 定容 |
D、 过滤 |
下列反应的离子方程式正确的是( )
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| B、用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
| C、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| D、氨水与醋酸反应:NH3?H2O+CH3COOH?CH3COO-+NH4++H2O |
下列关于NO的说法错误的是( )
| A、NO是红棕色气体 |
| B、放电氮气与氧气反应可生成NO |
| C、NO是有毒气体 |
| D、NO2与水反应有NO生成 |
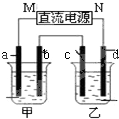 如图装置中甲烧杯盛放100mL 0.2mol?L-1的NaCl溶液,乙烧杯盛放100mL 0.5mol?L-1L的CuCl2溶液.a、b、c、d电极均为石墨,反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞溶液,观察到b电极附近首先变红.
如图装置中甲烧杯盛放100mL 0.2mol?L-1的NaCl溶液,乙烧杯盛放100mL 0.5mol?L-1L的CuCl2溶液.a、b、c、d电极均为石墨,反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞溶液,观察到b电极附近首先变红.