题目内容
10.要检验某溴乙烷中的溴元素,正确的实验方法是( )| A. | 加入氯水振荡,观察水层是否有红棕色出现 | |
| B. | 滴入AgNO3溶液,再加入稀HNO3,观察有无浅黄色沉淀生成 | |
| C. | 加入NaOH溶液共热,冷却后加入AgNO3溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入NaOH溶液共热,然后加入稀HNO3使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
分析 检验溴乙烷中溴元素,应在碱性条件下水解或在NaOH醇溶液中发生消去,再加入硝酸酸化,最后加入硝酸银,观察是否有黄色沉淀生成,以此来解答.
解答 解:A.氯水与溴乙烷不反应,不能检验,故A错误;
B.溴乙烷与硝酸银不反应,不能鉴别,故B错误;
C.冷却后先加硝酸至酸性,再加入AgNO3溶液,观察有无浅黄色沉淀生成,故C错误;
D.加入NaOH溶液共热,发生水解反应生成NaBr,然后加入稀HNO3使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成可检验,故D正确;
故选D.
点评 本题考查物质的检验和鉴别,为高频考点,把握有机物的结构与性质、卤素离子的检验方法为解答的关键,侧重分析与应用能力的考查,注意有机物的性质,题目难度不大.

练习册系列答案
相关题目
20.将Fe、FeO和Fe2O3的混合物m g加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08mol,放出的气体在标准状况下的体积为0.224L,则原混合物中氧元素的质量分数为( )
| A. | 20.5% | B. | 18.6% | C. | 17.6% | D. | 无法计算 |
1.下列物质沸点的比较,错误的是( )
| A. | 丙烷>乙烷 | B. | 丁烷>乙醇 | C. | 苯酚>苯 | D. | 1-氯丙烷>丙烷 |
18.下列各物质中,按熔点由高到低的顺序排列正确的是( )
| A. | CH4>SiH4>GeH4>SnH4 | B. | KCl>NaCl>MgCl2>MgO | ||
| C. | Rb>K>Na>Li | D. | 金刚石>SiC>Si>S |
5.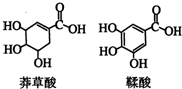 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸都能与溴水反应 | |
| B. | 两种酸遇三氯化铁溶液都显色 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 等物质的量的两种酸与足量金属钠反应产生氢气的量不相同 |
15.已知烯烃、炔烃在臭氧的作用下发生以下反应:
CH3-CH═CH-CH2-CH═CH2→CH3CHO+OHC-CH2-CHO+HCHO
CH3-C≡C-CH2-C≡CH-→CH3COOH+HOOCCH2COOH+HCOOH 某烃分子式为C10H10,在臭氧作用下发生反应:C10H10→CH3COOH+3HOOC-CHO+CH3CHO,
下列判断正确在是( )
CH3-CH═CH-CH2-CH═CH2→CH3CHO+OHC-CH2-CHO+HCHO
CH3-C≡C-CH2-C≡CH-→CH3COOH+HOOCCH2COOH+HCOOH 某烃分子式为C10H10,在臭氧作用下发生反应:C10H10→CH3COOH+3HOOC-CHO+CH3CHO,
下列判断正确在是( )
| A. | 其结构中含有4个碳碳双键,4个碳碳三键 | |
| B. | 分子中含有4个碳碳双键和2个碳碳三键 | |
| C. | 该烃结构简式是:CH3-C≡C-CH=CH-C≡C-CH=CH-CH3 | |
| D. | 其结构中含有2个碳碳双键,4个碳碳三键 |
2.下列实验能获得成功的是( )
| A. | 苯和浓溴水用铁做催化剂制溴苯 | |
| B. | 甲烷与氯气光照制得纯净的一氯甲烷 | |
| C. | 实验室用CaC2和饱和食盐水制备乙炔 | |
| D. | 将苯与浓硝酸混合共热制硝基苯 |
19.下列化合物中既有离子键又有极性键的是( )
| A. | MgBr2 | B. | NaOH | C. | K2O2 | D. | H2O2 |
20.现有三组混合液:①硝基苯和氢氧化钠溶液 ②苯和甲苯 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |