题目内容
在某100 mL混合溶液中,HNO3和H2SO4的物质的量浓度分别为0.400 mol·L-1和0.100 mol·L-1,向该混合溶液中加入1.92 g铜粉,加热使其充分反应,若反应前后溶液体积视作不变,反应后溶液中Cu2+的物质的量浓度为
- A.0.15 mol·L-1
- B.0.225 mol·L-1
- C.0.3 mol·L-1
- D.0.6 mol·L-1
B
溶液中n(H+)=0.1 L×0.4 mol·L-1+0.1 L×0.1 mol·L-1×2=0.06 mol
n(Cu)=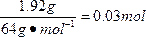
n( )=0.1 L×0.4 mol·L-1=0.04 mol
)=0.1 L×0.4 mol·L-1=0.04 mol
3Cu + 8H++ 2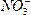 ====3Cu2++2NO↑+4H2O
====3Cu2++2NO↑+4H2O
0.03 mol 0.06 mol 0.04 mol
因n(H+)不足,故只消耗Cu: ×0.06=0.0225 mol
×0.06=0.0225 mol
c(Cu2+)= =0.225 mol·L-1
=0.225 mol·L-1
溶液中n(H+)=0.1 L×0.4 mol·L-1+0.1 L×0.1 mol·L-1×2=0.06 mol
n(Cu)=
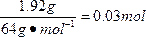
n(
 )=0.1 L×0.4 mol·L-1=0.04 mol
)=0.1 L×0.4 mol·L-1=0.04 mol3Cu + 8H++ 2
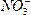 ====3Cu2++2NO↑+4H2O
====3Cu2++2NO↑+4H2O0.03 mol 0.06 mol 0.04 mol
因n(H+)不足,故只消耗Cu:
 ×0.06=0.0225 mol
×0.06=0.0225 molc(Cu2+)=
 =0.225 mol·L-1
=0.225 mol·L-1 
练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目