题目内容
技术的发展与创新永无止境,我国化工专家侯德榜改革国外路布兰、索尔维的纯碱生产工艺,使生产纯碱的成本明显降低.生产流程可简要表示如下图:

(1)向沉淀池中要通入CO2和氨气,应先通入 (填化学式).
(2)沉淀池中发生反应的化学方程式 ,煅烧炉中发生反应的化学方程式是 .
(3)向母液中通氨气后再加入细小食盐颗粒,冷却析出的副产品是 ,加入细小食盐颗粒的作用是 .
(4)写出路布兰制碱法的反应原理中属于氧化还原反应的化学方程式 ,该法与侯德榜制碱法相比的缺点是 (写出两点即可)
(5)候氏制碱法制得的纯碱中含有碳酸氢钠杂质.现用沉淀法测定纯碱的纯度,取m1g样品,加水溶解,再加过量的CaCl2溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为m2g.则此样品中的纯度表达式为: .

(1)向沉淀池中要通入CO2和氨气,应先通入
(2)沉淀池中发生反应的化学方程式
(3)向母液中通氨气后再加入细小食盐颗粒,冷却析出的副产品是
(4)写出路布兰制碱法的反应原理中属于氧化还原反应的化学方程式
(5)候氏制碱法制得的纯碱中含有碳酸氢钠杂质.现用沉淀法测定纯碱的纯度,取m1g样品,加水溶解,再加过量的CaCl2溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为m2g.则此样品中的纯度表达式为:
考点:氯碱工业
专题:
分析:(1)氨气极易溶于水,二氧化碳在水中的溶解度较小;
(2)饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体,煅烧碳酸氢钠分解生成碳酸钠、二氧化碳气体和水;
(3)根据反应方程式确定母液中的溶质,食盐中含有氯离子,加入食盐有利于氯化铵析出;
(4)碳的产物是二氧化碳,据此书写;依据化学方程式中物质的定量关系分别计算得到所求各量;布兰制碱法与其它两种制碱法工艺相比生产时需要高温消耗能源,需硫酸,硫酸具有腐蚀性,中间产物为CaS,废弃物长期堆积臭气四溢;
(5)此反应的原理为:碳酸钠与氯化钙反应生成碳酸钙沉淀.
(2)饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体,煅烧碳酸氢钠分解生成碳酸钠、二氧化碳气体和水;
(3)根据反应方程式确定母液中的溶质,食盐中含有氯离子,加入食盐有利于氯化铵析出;
(4)碳的产物是二氧化碳,据此书写;依据化学方程式中物质的定量关系分别计算得到所求各量;布兰制碱法与其它两种制碱法工艺相比生产时需要高温消耗能源,需硫酸,硫酸具有腐蚀性,中间产物为CaS,废弃物长期堆积臭气四溢;
(5)此反应的原理为:碳酸钠与氯化钙反应生成碳酸钙沉淀.
解答:
解:(1)二氧化碳在水中的溶解度较小,氨气极易溶于水,所以应该先通氨气有利于吸收二氧化碳,故答案为:NH3;
(2)氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,碳酸氢钠分解生成碳酸钠、二氧化碳、水,化学方程式为:2NaHCO3
Na2CO3+CO2↑+H2O,故答案为:NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓;2NaHCO3
Na2CO3+CO2↑+H2O;
(3)根据NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程图知,母液中溶质为氯化铵,故向母液中通氨气后再加入细小食盐颗粒,冷却析出的副产品是:NH4Cl,食盐中含有氯离子,加入食盐有利于氯化铵析出,故答案为:NH4Cl;增大Cl-浓度,使NH4Cl更多析出;
(4)碳被氧化生成二氧化碳,此时所发生的反应的化学方程式:Na2SO4+2C
Na2S+2CO2↑,布兰制碱法用氯化钠与硫酸反应制硫酸钠,用焦炭还原硫酸钠得硫化钠,用硫化钠与石灰石反应制碳酸钠,原料需硫酸,硫酸具有腐蚀性,硫酸对设备腐蚀严重,生产时需要高温消耗能源成本较高,中间产物为CaS,废弃物长期堆积臭气四溢,故答案为:Na2SO4+2C
Na2S+2CO2↑;生产时需要高温、硫酸对设备腐蚀严重、CaS废弃物长期堆积臭气四溢、成本较高;
(5)此时发生的反应为:Na2CO3+CaCl2=CaCO3+2NaCl
106 100
x m2
解x=
,故纯碱的纯度为:
×100%=
%,故答案为:
%.
(2)氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,碳酸氢钠分解生成碳酸钠、二氧化碳、水,化学方程式为:2NaHCO3
| ||
| ||
(3)根据NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程图知,母液中溶质为氯化铵,故向母液中通氨气后再加入细小食盐颗粒,冷却析出的副产品是:NH4Cl,食盐中含有氯离子,加入食盐有利于氯化铵析出,故答案为:NH4Cl;增大Cl-浓度,使NH4Cl更多析出;
(4)碳被氧化生成二氧化碳,此时所发生的反应的化学方程式:Na2SO4+2C
| ||
| ||
(5)此时发生的反应为:Na2CO3+CaCl2=CaCO3+2NaCl
106 100
x m2
解x=
| 106m2 |
| 100 |
| ||
| m1 |
| 106m2 |
| m1 |
| 106m2 |
| m1 |
点评:本题主要考查了实验方案的设计,明确物质的性质是解本题关键,了解制备原理,知道常见物质分离的方法,难度中等.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案
相关题目
下列化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 | ||
B、S2-的结构示意图: | ||
C、中子数为20的氯原子:
| ||
D、羟基的电子式: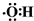 |
由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为( )
| A、0.1 mol |
| B、大于或等于0.2 mol且小于0.3 mol |
| C、等于0.2 mol |
| D、大于0.1 mol且小于0.3 mol |





 据此推断经反应④得到一种副产物,其核磁共振氢谱有
据此推断经反应④得到一种副产物,其核磁共振氢谱有



