题目内容
4.下列事故处理,不正确的是( )| A. | 误食铜盐立即喝牛奶和蛋清 | |
| B. | 镁带和金属钠着火时用沙子灭火 | |
| C. | 皮肤上沾有苯酚,应立即用大量稀NaOH冲洗 | |
| D. | 碱液流到木桌上,立即往碱里加适量的稀醋酸中和,然后用水冲洗 |
分析 A.铜盐能使蛋白质变性,牛奶或蛋清的主要成分为蛋白质;
B.钠着火生成过氧化钠,与二氧化碳、水都反应;
C.氢氧化钠有强腐蚀性;
D.碱液用稀醋酸中和.
解答 解:A.铜盐能使蛋白质变性,牛奶或蛋清的主要成分为蛋白质,牛奶或蛋清中的蛋白质变性从而保护人体中蛋白质,故A正确;
B.钠性质很活泼,能和水、氧气反应,所以为防止钠燃烧,必须隔绝空气和水,镁带和金属钠着火时一般用细沙覆盖灭火,故B正确;
C.氢氧化钠有强腐蚀性,会损伤皮肤,应用酒精溶液洗去,故C错误;
D.较多量的碱液泼在实验台上,立即用适量的稀醋酸中和,以除去碱液,然后用水冲洗,用抹布擦干,故D正确.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验安全、蛋白质变性等,物质性质及实验基本技能的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
14.以下微粒通常只具有氧化性的是( )
| A. | Fe | B. | Fe2+ | C. | Fe3+ | D. | H2 |
12.实现下列操作的正确方法依次是( )
①分离植物油和水 ②去除KNO3溶液中少量的NaCl杂质 ③用四氯化碳提取溴水中的溴.
①分离植物油和水 ②去除KNO3溶液中少量的NaCl杂质 ③用四氯化碳提取溴水中的溴.
| A. | 蒸发、萃取、分液 | B. | 萃取、过滤、结晶 | C. | 过滤、蒸发、萃取 | D. | 分液、结晶、萃取 |
19.下列有关氯气的描述,不正确的是( )
| A. | 氯气是一种密度比空气大的有毒气体 | |
| B. | 液氯可储存于钢瓶中,便于运输和使用 | |
| C. | 常温下,1体积水能溶解2体积氯气 | |
| D. | 过量的铁与氯气反应生成氯化亚铁 |
9.某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:下列叙述错误的是( )
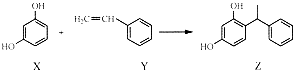

| A. | X、Z均能与FeCl3 形成紫色的溶液 | |
| B. | 1molZ最多能消耗3mol溴水 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
5.化工生产中原料转化与利用非常重要,现有反应:CCl4+H2?CHCl3+HCl,查阅资料可知沸点:CCl4为77℃,CHCl3为61.2℃.在密闭容器中,该反应达到平衡后,测得下表数据(假设不考虑副反应).
(1)在100℃时,此反应的化学平衡常数表达式为$\frac{c(CHC{l}_{3})×c(HCl)}{c(CC{l}_{4})×c({H}_{2})}$;在110℃时的平衡常数为1.
(2)在实验2中,若1小时后反应达到平衡,则H2的平均反应速率为0.5mol/(L.h),在此平衡体系中再加入0.5molCCl4和1.0molHCl,平衡将向逆 方向移动.(填正、逆或不移动)
(3)实验1中,CCl4的转化率a>50%(填“>”、“=”或“<”).实验3中,b的值D (填字母序号).
A.等于50% B.大于50% C.小于50% D.由本题所给资料无法判断.
| 实验 序号 | 温度℃ | 初始CCl4浓度 (mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | b |
(2)在实验2中,若1小时后反应达到平衡,则H2的平均反应速率为0.5mol/(L.h),在此平衡体系中再加入0.5molCCl4和1.0molHCl,平衡将向逆 方向移动.(填正、逆或不移动)
(3)实验1中,CCl4的转化率a>50%(填“>”、“=”或“<”).实验3中,b的值D (填字母序号).
A.等于50% B.大于50% C.小于50% D.由本题所给资料无法判断.