题目内容
下列关于物质性质的比较,不正确的是( )
| A、酸性强弱:HClO4>HBrO4>HIO4 |
| B、氢化物稳定性:HF>H2O>NH3 |
| C、沸点高低:HF>HBr>HCl |
| D、密度大小:K>Na>Li |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.元素的非金属性越强,对应的氢化物越稳定;
C.氢化物的分子量越大,沸点越高,含有氢键的沸点较高;
D.碱金属的密度呈递增趋势,钠钾反常.
B.元素的非金属性越强,对应的氢化物越稳定;
C.氢化物的分子量越大,沸点越高,含有氢键的沸点较高;
D.碱金属的密度呈递增趋势,钠钾反常.
解答:
解:A.非金属性:Cl>Br>I,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,即酸性强弱:HClO4>HBrO4>HIO4,故A正确;
B.元素的非金属性越强,对应的氢化物越稳定,非金属性:F>O>N,则氢化物稳定性:HF>H2O>NH3,故B正确;
C.氢化物的分子量越大,沸点越高,含有氢键的沸点较高,所以沸点高低:HF>HBr>HCl,故C正确;
D.碱金属的密度呈递增趋势,钠钾反常,密度大小:Na>K>Li,故D错误;
故选D.
B.元素的非金属性越强,对应的氢化物越稳定,非金属性:F>O>N,则氢化物稳定性:HF>H2O>NH3,故B正确;
C.氢化物的分子量越大,沸点越高,含有氢键的沸点较高,所以沸点高低:HF>HBr>HCl,故C正确;
D.碱金属的密度呈递增趋势,钠钾反常,密度大小:Na>K>Li,故D错误;
故选D.
点评:本题考查元素周期律的递变规律,题目难度不大,注意把握元素的递变规律以及与对应单质、化合物的性质的关机以及比较角度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、氯化氢气体 |
| B、CO2 |
| C、Cl2 |
| D、氯化钠 |
下列说法正确的是( )
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、鸡蛋清中加入CuSO4溶液产生盐析 |
| C、乙酸乙酯、油脂与NaOH溶液反应均有乙醇生成 |
| D、石油分馏可得到汽油、煤油等 |
常温下,下列各组气体能共存(即不发生反应)的是( )
| A、NH3和HCl |
| B、NH3和SO2 |
| C、N2和O2 |
| D、NO和O2 |
用下图所示装置进行实验,装置正确且设计合理的是( )
A、 实验室制硝基苯 |
B、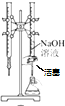 用已知浓度的NaOH溶液测定盐酸浓度的实验 |
C、 在铁制品表面镀锌操作 |
D、 称取一定量的NaOH固体 |
下列说法不正确的是( )
| A、乙醇、乙醛、乙酸都能与H2O形成分子间氢键 |
| B、丙烯中最多有7个原子共平面 |
| C、乙醇与金属钠反应比水与金属钠反应更剧烈,羟基H活性更高 |
D、乙酸、甲酸甲酯和羟基乙醛 互为同分异构体 互为同分异构体 |