题目内容
19.根据下面的反应路线及所给信息填空.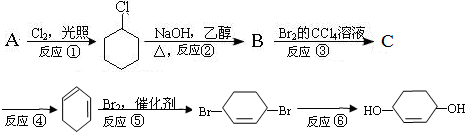
(1)在①~⑥的各步反应中,属于取代反应的有①⑥,属于加成反应的有③⑤
(2)反应④所用的试剂和条件是NaOH的乙醇溶液、加热
(3)反应③的化学方程式是
(4)反应⑥的化学方程式是
 .
.
分析 A和氯气光照得到 ,A为环己烷
,A为环己烷 ,反应为
,反应为 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,一氯环己烷在氢氧化钠、乙醇、加热条件下发生消去反应得到B,B为
+HCl,一氯环己烷在氢氧化钠、乙醇、加热条件下发生消去反应得到B,B为 ,反应②为:
,反应②为: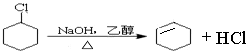 ;
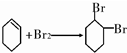
; 与溴的四氯化碳发生加成反应,反应③为:
与溴的四氯化碳发生加成反应,反应③为: ,卤代烃发生消去反应生成烯烃
,卤代烃发生消去反应生成烯烃 ,反应④为:
,反应④为: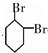 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O,与溴在催化剂的作用下发生加成反应生成
+2NaBr+2H2O,与溴在催化剂的作用下发生加成反应生成 ,反应⑤为:
,反应⑤为: +Br2$\stackrel{催化剂}{→}$
+Br2$\stackrel{催化剂}{→}$ ,发生卤代烃的水解生成
,发生卤代烃的水解生成 ,反应⑥为:
,反应⑥为: ,
,
(1)根据反应①为取代反应,反应②为消去反应,反应③为加成反应,反应④为消去反应,反应⑤为加成反应,反应⑥为取代反应解答;
(2)根据前后物质,反应④为卤代烃的消去反应,需NaOH的乙醇溶液、加热条件;
(3)反应③为烯烃的加成反应生成卤代烃;
(4)反应⑥卤代烃的水解生成醇,据此书写方程式;
解答 解:A和氯气光照得到 ,A为环己烷,一氯环己烷在氢氧化钠、乙醇、加热条件下得到B,B为
,A为环己烷,一氯环己烷在氢氧化钠、乙醇、加热条件下得到B,B为 ,
, 与溴的四氯化碳反应生成C,C为
与溴的四氯化碳反应生成C,C为 ,卤代烃发生消去反应生成烯烃
,卤代烃发生消去反应生成烯烃 ,与溴在催化剂的作用下反应生成
,与溴在催化剂的作用下反应生成 ,发生卤代烃的水解生成
,发生卤代烃的水解生成 ,
,
流程反应为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,
+HCl, ,
, ,
, +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O,
+2NaBr+2H2O, +Br2$\stackrel{催化剂}{→}$
+Br2$\stackrel{催化剂}{→}$ ,
, ,
,
(1)反应①为环烷烃的取代反应,反应②为卤代烃的消去反应,反应③为烯烃的加成反应,反应④为卤代烃的消去反应,反应⑤为烯烃的加成反应,反应⑥为卤代烃的水解,为取代反应.
故答案为:①⑥;③⑤;
(2)反应④为卤代烃的消去反应,反应条件为氢氧化钠、乙醇、加热,
故答案为:氢氧化钠、乙醇、加热;
(3)反应③为烯烃的加成反应,化学方程式是: ,
,
故答案为: ;
;
(4)反应⑥卤代烃的水解,方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的合成,明确反应条件与反应类型的关系来推出各物质是解答本题的关键,本题重点考查了卤代烃的消去反应、烯烃的加成反应和卤代烃的取代反应及相关方程式的书写,题目难度中等.

| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| C. | PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | 开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题 |
| A. | Na在足量O2中燃烧,消耗1mol O2时转移的电子数是4×6.02×1023 | |
| B. | 标准状况下,6.72L NO2与水分子充分反应转移的电子数目为0.1NA | |
| C. | 盐酸和醋酸的混合溶液pH=1,该溶液中c(H+)=0.1 mol/L | |
| D. | 1 L 0.1 mol/L NH4Cl溶液中的NH4+数是0.1×6.02×1023 |
| A. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热--检验混合物中是否含有甲醛 | |
| B. | 向CH3CH2Br中滴入AgNO3溶液以检验溴元素 | |
| C. | 苯不能与溴水发生取代反应,用苯能萃取溴的四氯化碳溶液中的溴 | |
| D. | 利用核磁共振氢谱,可以鉴别CH3OCH3和CH3CH2OH |
| A. | 78gNa2O2晶体中所含阴、阳离子个数均为2NA | |
| B. | HBr的电子式为H+( )- )- | |
| C. | 3.4g氨气中含有0.6NA个N-H键 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
| A. | X位于元素周期表中第2周期ⅤA族 | |
| B. | X元素有-3、+5两种化合价 | |
| C. | X元素在元素周期表中的族序数肯定为奇数 | |
| D. | X元素最高价氧化物对应的水化物可以表示为H3XO4 |
| A. | 2CH3OH+3O2→2CO2+4H2O | B. | NaOH+HCl=NaCl+H2O | ||
| C. | Zn+2HCl=ZnCl2+H2↑ | D. | 4Al+3O2+6H2O=4Al(OH)3 |

