题目内容
在25℃下,将0.02mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,下列混合液中各种离子浓度的关系不正确的是( )
| A、C(Cl-)+C(OH-)=C(H+)+C(NH4+) |
| B、2C(Cl-)=C(NH4+)+C(NH3﹒H2O) |
| C、C(NH4+)+2C(H+)=C(NH3﹒H2O)+2C(OH-) |
| D、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
考点:离子浓度大小的比较,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:在25℃下,将0.02mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,溶液中的溶质是等物质的量浓度的NH3﹒H2O、NH4Cl,一水合氨电离程度大于铵根离子水解程度,导致溶液呈碱性,溶液中存在电荷守恒和物料守恒,据此分析解答.
解答:
解:在25℃下,将0.02mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,溶液中的溶质是等物质的量浓度的NH3﹒H2O、NH4Cl,一水合氨电离程度大于铵根离子水解程度,导致溶液呈碱性,
A.根据电荷守恒得C(Cl-)+C(OH-)=C(H+)+C(NH4+),故A正确;
B.根据物料守恒得2C(Cl-)=C(NH4+)+C(NH3﹒H2O),故B正确;
C.根据电荷守恒得C(Cl-)+C(OH-)=C(H+)+C(NH4+)、根据物料守恒得2C(Cl-)=C(NH4+)+C(NH3﹒H2O),所以得C(NH4+)+2C(H+)=C(NH3﹒H2O)+2C(OH-),故C正确;
D.一水合氨电离程度大于铵根离子水解程度,导致溶液呈碱性,则C(H+)<C(OH-),根据电荷守恒得C(Cl-)<C(NH4+),故D错误.
故选D.
A.根据电荷守恒得C(Cl-)+C(OH-)=C(H+)+C(NH4+),故A正确;
B.根据物料守恒得2C(Cl-)=C(NH4+)+C(NH3﹒H2O),故B正确;
C.根据电荷守恒得C(Cl-)+C(OH-)=C(H+)+C(NH4+)、根据物料守恒得2C(Cl-)=C(NH4+)+C(NH3﹒H2O),所以得C(NH4+)+2C(H+)=C(NH3﹒H2O)+2C(OH-),故C正确;
D.一水合氨电离程度大于铵根离子水解程度,导致溶液呈碱性,则C(H+)<C(OH-),根据电荷守恒得C(Cl-)<C(NH4+),故D错误.
故选D.
点评:本题考查了离子浓度大小比较,根据两种物质的量之间的关系式确定溶液中的溶质,再根据溶质的性质确定元素酸碱性,结合守恒思想分析解答,题目难度中等.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案
相关题目
下列离子方程式正确的是( )
| A、石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B、硫酸氢钠溶液中加入氢氧化钡溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C、氧化铜与稀硫酸反应:2H++O2-=H2O |
| D、碳酸氢钠溶液中加入盐酸:CO32-+2H+=CO2↑+H2O |
下列粒子不具有还原性的是( )
| A、Na+ |
| B、H2 |
| C、S2- |
| D、Fe2+ |
西维因是一种高效低毒杀虫剂,在碱性条件下可水解:有关说法正确的是( )
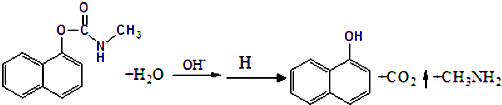

| A、西维因分子式为C12H10NO2 |
| B、反应后的溶液经酸化,不可用FeCl3溶液检验西维因是否已经发生水解 |
| C、水解后的两种有机产物,各有一种官能团 |
| D、西维因分子中至少有21个原子共平面 |
因为自然界的水含有很多杂质,要经过一定处理措施后才能饮用.下列处理过程中没有发生了物理变化的是( )
| A、过滤悬浮物质 |
| B、投药品,消毒杀菌 |
| C、用活性炭吸附杂质 |
| D、制成蒸馏水 |
一定温度压强下的下列各组物质总物质的量保持不变时,使各组分以任意比混合后充分燃烧,消耗氧气的物质的量相等的一组是 ( )
①乙醇和乙醚 ②丙醛和丙炔 ③甲烷和甲酸甲酯 ④乙炔和乙酸.
①乙醇和乙醚 ②丙醛和丙炔 ③甲烷和甲酸甲酯 ④乙炔和乙酸.
| A、②③ | B、①② | C、③④ | D、②④ |
“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥缩聚反应 ⑦酯化反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥缩聚反应 ⑦酯化反应.
| A、②⑤ | B、④⑤ | C、⑥⑦ | D、①③ |
下列事实与氢键无关的是( )
| A、液态氟化氢中有三聚氟化氢(HF)3分子存在 |
| B、冰的密度比液态水的密度小 |
| C、乙醇能与水以任意比混溶而甲醚(CH3-O-CH3)难溶于水 |
| D、H2O比H2S稳定 |