题目内容
(本题共13分)甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。
| 步骤 | 操作 | 现象 |
| Ⅰ | 向2mL 1 mol·L-1FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黄色变为红褐色,并有少量刺激性气味的气体逸出 |
(2)分析红褐色产生的原因。
① 甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,请用化学平衡移动原理解释溶液呈红褐色的原因:________。
② 乙同学认为可能是发生了氧化还原反应,其中Fe3+ →Fe2+ ;请写出Fe3+ 跟SO32-反应的离子方程式
______________。
乙同学查阅资料得知:
1.Fe2+与SO32-反应生成墨绿色的絮状沉淀FeSO3;
2.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色。
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅱ | 用激光笔照射步骤I中的红褐色溶液 | 出现“丁达尔效应” |
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅲ | 向1 mol?L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黄色变为红褐色 |
| Ⅳ | 用激光笔照射步骤Ⅲ中的红褐色溶液 | 没有出现“丁达尔效应” |
a.K3[Fe(CN)6] 溶液 b.KSCN溶液 c.KMnO4溶液
② 请用离子方程式和必要的文字说明步骤Ⅲ中出现红褐色的原因 。
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
解析试题分析:(1)氯化铁是强酸弱碱盐,铁离子水解溶液显酸性,因此常温下,FeCl3溶液的pH<7。
(2)① 在氯化铁溶液中存在铁离子的水解平衡:Fe3++3H2O Fe(OH)3+3H+,加入Na2SO3后,消耗氢离子,溶液中c(H+)下降,平衡正向移动,生成Fe(OH)3。
Fe(OH)3+3H+,加入Na2SO3后,消耗氢离子,溶液中c(H+)下降,平衡正向移动,生成Fe(OH)3。
②铁离子具有氧化性,亚硫酸钠具有还原性,二者可以发生氧化还原反应,离子方程式为2Fe3+ + SO32- +H2O==2Fe2+ +SO42-+2H+。
(3)由于FeSO3和FeCl3混合后即使不反应,混合溶液也可能出现“丁达尔效应”。
(4)①由于溶液显红褐色,虽然亚铁离子能与高锰酸钾溶液反应,但现象不明显,所以检验亚铁离子的试剂应该选择K3[Fe(CN)6] 溶液,实验现象是溶液中产生蓝色沉淀,答案选a。
②在溶液中铁离子与SO2发生氧化还原反应:2Fe3+ + SO2 + 2H2O =2Fe2+ + SO2- 4 + 4H+,生成的亚铁离子与SO2继续反应:Fe2+ + SO2 +H2O=FeSO3↓ + 2H+(或2Fe3+ + 3SO2 + 4H2O =2FeSO3↓+ SO2- 4 + 8H+),生成的FeSO3与剩余的FeCl3溶液混合而呈现红褐色。
考点:考查离子检验、实验方案设计与评价

 阅读快车系列答案
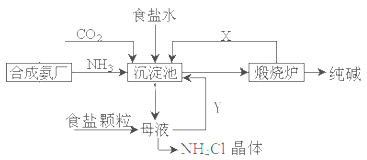
阅读快车系列答案已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O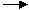 Y+H2
Y+H2 ↑;Z+H2O
↑;Z+H2O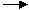 W+O2↑(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
W+O2↑(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
| A.X>Y Z>W | B.X<Y Z<W |
| C.X>Y Z<W | D.X<Y Z>W |
(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。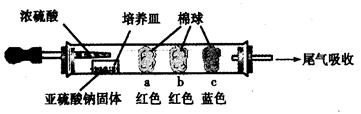
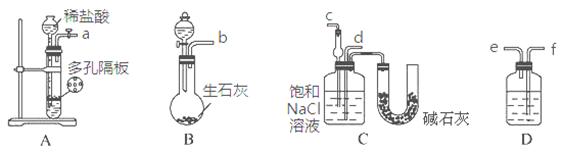
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | | 棉球变白,微热后又恢复红色 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | | 棉球变为白色 | 该气体具有 (选填“氧化性”或“还原性”) |
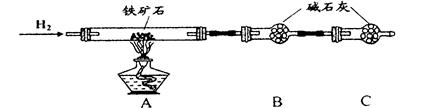
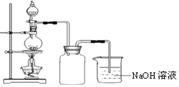
实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
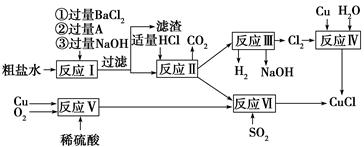
实验二:铁矿石中含铁量的测定
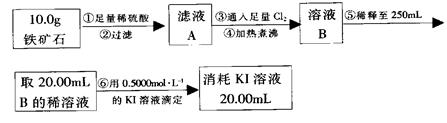
(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
A.滴定管用蒸馏水洗涤后再用待装液润洗
B.锥形瓶需要用待测液润洗
C.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为